题目内容
5.下列说法不正确的是( )| A. | 用浓硝酸与蛋白质的颜色反应鉴别部分蛋白质 | |
| B. | 用分液漏斗从石油里分离出汽油、煤油和石蜡 | |
| C. | 可用水鉴别苯、四氯化碳、乙醇三种无色液体 | |
| D. | 用灼烧闻气味的方法可区别纯棉织物和纯毛织物 |
分析 A.带有苯环的蛋白质与硝酸可发生颜色反应;
B.汽油、煤油和石蜡混溶,应用蒸馏的方法分离;
C.苯的密度小于水,四氯化碳的密度大于水,乙醇与水混溶;
D.纯棉的成分就是纤维素纤维,纯毛织物是蛋白质纤维.
解答 解:A.带有苯环的蛋白质与硝酸可发生颜色反应,可鉴别,故A正确;
B.汽油、煤油和石蜡混溶,应用蒸馏的方法分离,故B错误;
C.苯的密度小于水分层在水溶液上层,四氯化碳的密度大于水分层在溶液下面,乙醇与水混溶不分层,故可以用水鉴别,故C正确;
D.纯棉的成分就是纤维素纤维,跟纸张的化学成分完全一样.所以,燃烧起来就是烧纸张的气味.纯毛的都是蛋白质纤维,跟毛发的化学成分完全一样.所以烧起来有烧焦羽毛的气味,故D正确.
故选B.
点评 本题考查较为综合,涉及气体的制备、物质的检验以及物质的检验等操作,侧重于学生的分析能力和实验能力的考查,注意把握相关实验操作的注意事项,结合物质的性质的异同解答,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.在体积为1L的两个恒容密闭容器中,分别充入1molCO和1molH2O(g)的混合气体,进行如下化学反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
(1)1100℃时,前10min该反应的化学反应速率v(CO2)=0.025mol/(L.min).
(2)计算1100℃时该反应的化学平衡常数K=$\frac{4}{9}$.
(3)能判断该反应是否达到化学平衡状态的依据是bc.
(a)容器中压强不变
(b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O)
(d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡向右移动(选填“向右”或“向左”或“不”),再达到平衡时,H2百分含量不变(选填“增大”或“减小”或“不变”).
| 0min | 10min | 20min | 30min | 40min | 50min | |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
(2)计算1100℃时该反应的化学平衡常数K=$\frac{4}{9}$.
(3)能判断该反应是否达到化学平衡状态的依据是bc.
(a)容器中压强不变
(b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O)
(d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡向右移动(选填“向右”或“向左”或“不”),再达到平衡时,H2百分含量不变(选填“增大”或“减小”或“不变”).
16.根据陈述的知识,类推得出的结论正确的是( )
| A. | 镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O | |
| B. | 乙烯(CH2=CH2)可使酸性高锰酸钾溶液褪色,则丙烯(CH3-CH=CH2)也可以使其褪色 | |
| C. | CO2和SiO2化学式相似,则CO2与SiO2的物理性质也相似 | |
| D. | 金刚石的硬度大,则C60的硬度也大 |
20.下列有关元素非金属性的比较,正确的是( )
| A. | 进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱 | |
| B. | HCl溶液的酸性比H2S溶液的酸性强,则氯元素的非金属性比硫强 | |
| C. | H2O的沸点高于H2S,则氧元素的非金属性强于硫元素 | |
| D. | 浓H2SO4的氧化性强于HClO4,可确定硫和氯两种元素的非金属性强弱 |
10.在标准状况下,进行甲、乙、丙三组镁铝合金与盐酸反应实验,三组实验的有关数据如表:
试完成下列问题:
(1)①甲组实验中,盐酸过量(填“过量”“适量”或“不足量”),理由是HCl的物质的量一定,甲中合金质量小于乙中合金质量,且甲中生成气体体积小于乙中气体体积
②乙组实验中,盐酸不足(填“过量”“适量”或“不足量”),理由是生成336mL氢气需要合金的质量为255mg×$\frac{336mL}{280mL}$=306mg<385mg
(2)求合金中镁、铝的物质的量之比,题中可作计算依据的数据是甲,求得镁、铝的物质的量之比是1:1;
(3)求HCl的物质的量.
| 组别 | 镁铝合金质量.mg | HCl物质的量/mol | 氢气的体积/mL |
| 甲 | 255 | X | 280 |
| 乙 | 385 | X | 336 |
| 丙 | 459 | X | 336 |
(1)①甲组实验中,盐酸过量(填“过量”“适量”或“不足量”),理由是HCl的物质的量一定,甲中合金质量小于乙中合金质量,且甲中生成气体体积小于乙中气体体积
②乙组实验中,盐酸不足(填“过量”“适量”或“不足量”),理由是生成336mL氢气需要合金的质量为255mg×$\frac{336mL}{280mL}$=306mg<385mg
(2)求合金中镁、铝的物质的量之比,题中可作计算依据的数据是甲,求得镁、铝的物质的量之比是1:1;
(3)求HCl的物质的量.
17.已知有四种有机物A、B、C、D,其分子式均为C3H6O2,分子结构中均有甲基把它们分别进行实验并记录现象如下:
则A、B的结构简式为:ACH3CH2COOH;BCH3CHOHCHO;C、D的名称:C甲酸乙酯;D乙酸甲酯.
| 有机物 | 氢氧化钠 | 银氨溶液 | 新制氢氧化铜 | 金属钠 |
| A | 发生中和反应 | 不反应 | 溶解 | 放出氢气 |
| B | 不反应 | 发生银镜反应 | 生成红色沉淀 | 放出氢气 |
| C | 发生水解反应 | 发生银镜反应 | 生成红色沉淀 | 不反应 |
| D | 发生水解反应 | 不反应 | 不反应 | 不反应 |
15.法国化学家伊夫•肖万获2005年诺贝尔化学奖.他发现了烯烃里的碳-碳双键会被拆散、重组,形成新分子,这种过程被命名为烯烃复分解反应.烯烃复分解反应可形象地描述为交换舞伴.(如图所示)
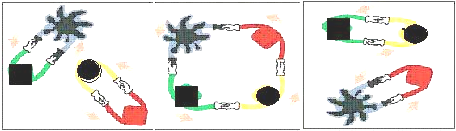
烯烃复分解反应中的催化剂是金属卡宾(如CH2=M),金属卡宾与烯烃分子相遇后,两对舞伴会暂时组合起来,手拉手跳起四人舞蹈.随后它们“交换舞伴”,组合成两个新分子,其中一个是新的烯烃分子,另一个是金属原子和它的新舞伴.后者会继续寻找下一个烯烃分子,再次“交换舞伴”.把C6H5CH2CH=CH2与CH2=M在一定条件下混合反应,下列产物不可能存在的是( )

烯烃复分解反应中的催化剂是金属卡宾(如CH2=M),金属卡宾与烯烃分子相遇后,两对舞伴会暂时组合起来,手拉手跳起四人舞蹈.随后它们“交换舞伴”,组合成两个新分子,其中一个是新的烯烃分子,另一个是金属原子和它的新舞伴.后者会继续寻找下一个烯烃分子,再次“交换舞伴”.把C6H5CH2CH=CH2与CH2=M在一定条件下混合反应,下列产物不可能存在的是( )
| A. | C6H5CH2CH=M | B. | CH2=CH2 | ||
| C. | C6H5CH2CH2C6H5 | D. | C6H5CH2CH=CHCH2C6H5 |
