题目内容
10.丹参素能明显抑制血小板的聚集,其结构如图所示,下列说法正确的是( )
| A. | 丹参素分子中有四种官能团,它与苯甲酸不是互为同系物 | |
| B. | 丹参素分子中C原子上的H被取代,所得一氯代物有4种 | |
| C. | 在Ni催化下1 mol丹参素最多可与4 mol H2发生加成反应 | |
| D. | 等量的丹参在一定条件下分别与足量Na、NaOH溶液反应,消耗两者的物质的量之比为4:3 |
分析 由结构可知,分子中含酚-OH、醇-OH、-COOH,结合酚、醇、羧酸的性质来解答.
解答 解:A.丹参素分子中有3种官能团,它与苯甲酸含官能团不同,二者不互为同系物,故A错误;
B.结构不对称,C原子上的H被取代,所得一氯代物有5种,故B错误;
C.只有苯环与氢气发生加成反应,1 mol丹参素最多可与3 mol H2发生加成反应,故C错误;
D.酚-OH、醇-OH、-COOH均与Na反应,酚-OH、-COOH与NaOH反应,则等量的丹参在一定条件下分别与足量Na、NaOH溶液反应,消耗两者的物质的量之比为4:3,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意酚、醇、羧酸的性质,题目难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
1.一定条件下,温度对有机污染物P-CP降解反应的影响如图所示.下列判断不正确的是( )
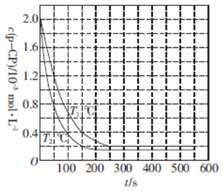

| A. | T1<T2 | |
| B. | p-CP降解反应是吸热反应 | |
| C. | 其他条件相同时,温度越高,反应速率越快 | |
| D. | T1℃时,在50〜150 s之间p-CP的平均降解速率为1.6×10-5 mol•L-1•s-1 |
18.下列各组粒子互为等电子体,且中心原子均进行sp3杂化的是( )
| A. | N3-与CO2 | B. | BF3和C O32- | C. | NO2+与CO2 | D. | H3O+与NH3 |
5.下列事实和解释正确的是( )
| A. | 锌与稀盐酸反应,加入NaCl固体后反应速率加快是因为增大了Cl-的浓度 | |
| B. | 面粉厂内要禁止明火是因为固体表面积大会加快反应速率 | |
| C. | 5%的H2O2中加入MnO2粉末后分解速率迅速加快是因为MnO2粉末降低了反应的焓变 | |
| D. | 锌与稀盐酸反应滴入CuSO4稀溶液反应速率变慢是因为CuSO4溶液中的水降低了硫酸的浓度 |
11.下列说法正确的是A( )
| A. | 电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离 | |
| B. | SO2水溶液能导电性,SO2是电解质,BaSO4水溶液不导电是非电解质 | |
| C. | 酸、碱和盐类都属于电解质,其他化合物都是非电解质 | |
| D. | Cu能导电所以Cu是电解质 |
8.Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.亚铁氰化钾K4[Fe(CN)6]中不包含下列哪种化学键 ( )
| A. | 极性键 | B. | 非极性键 | C. | 配位键 | D. | σ键 | ||||
| E. | π键 | F. | 离子键. |
9.关于卤素(F、Cl、Br、I)的性质的叙述,错误的是( )
| A. | 卤素单质的密度逐渐增大 | |
| B. | 将氯水加到KI淀粉溶液中,溶液变蓝 | |
| C. | 除了I2外,其它卤素单质都能将Fe氧化到+3价 | |
| D. | F2能从NaCl溶液中置换出Cl2 |
