题目内容
(8分)氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:
SiO2+ C+ N2 Si3N4+ CO
Si3N4+ CO
根据题意完成下列各题:
(1)配平上述化学反应方程式。
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了20mol氮气,反应生成了5mol一氧化碳,此时混合气体的平均相对分子质量是 。
(3)分析反应可推测碳、氮气的氧化性:C N2(填“>”“<”“=”)。
(4)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是 。
| A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备 |
| B.在电子工业上制成耐高温的电的良导体 |
| C.研发氮化硅的全陶发动机替代同类型金属发动机 |
| D.氮化硅陶瓷的开发受到资源的限制,没有发展前途 |
(共8分) (1) 3 6 2 1 6(2分) (2) 28(2分) (3) < (2分) (4) AC(2分)
解析试题分析:(1)Si的化合价前后未变,N的化合价由0降为-3,C的化合价由0升为+2,生成1个Si3N4化合价降低12,生成1个CO化合价升高2,根据化合价升降总数相等以及质量守恒得,3SiO2+6C+2N2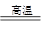 Si3N4+6CO;
Si3N4+6CO;
(2)生成了5mol一氧化碳,需要氮气是5/3mol,剩余氮气是55/3mol,但是由于CO与N2均为28g/mol,所以不管是何种比例,平均相对分子质量为28;
(3)在反应中碳化合价升高,做还原剂,氮气化合价降低,得电子,做氧化剂;所以碳的氧化性比氮气小;
(4)氮化硅陶瓷的机械强度高,硬度大,化学性质稳定,耐高温,说明是原子晶体,不能导电,B项错误;氮化硅的原料来源广,开发不会受到资源的限制,D项错误。
考点:考查氧化还原反应方程式的配平、平均相对分子质量的计算、原子晶体的性质。
点评:方程式配平、计算及氮化硅的性质,难度较小。

| ||
| A、氮化硅陶瓷可用于制造汽车发动机 |
| B、氮化硅中氮元素的化合价为─3 |
| C、氮化硅陶瓷属于新型无机非金属材料 |
| D、氮化硅不会与任何酸发生反应 |
| ||
(1)该反应中的氧化产物是
(2)800℃下,该反应的平衡常数表达式K=
(3)已知:该反应K800℃>K 850℃,则该反应是
(4)一定温度下,在2L密闭容器内,充入一定量SiO2、C、N2进行上述反应,N2的物质的量随时间(t)的变化如下表:
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(N2)/mol | 2.00 | 1.40 | 1.12 | 1.00 | 1.00 | 1.00 |
(5)若压缩(4)中的密闭体系,则上述平衡向
(6)能使SiO2的转化率增大的措施是
A.及时分离出CO气体 B.降低温度 C.增加C的初始量 D.使用适宜催化剂.
