题目内容
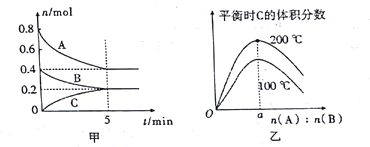
【题目】在4 L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
A. 200 ℃时,该反应的平衡常数为6.25L2/mol2
B. 由甲图和乙图可知,反应xA(g)+yB(g)![]() zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
C. 200℃时,向容器中加入2molA 和1molB,达到平街时C的体积分数大于0.25
D. 当外界条件由200℃降温到100℃,原平衡一定被破坏,且正反应速率均增大,逆反应速率减小
【答案】C
【解析】根据图甲,A、B、C物质的量随时间的变化分别是0.4mol、0.2mol、0.2mol;容器中发生反应的方程式是2A(g)+B(g)![]() C(g)。
C(g)。
200 ℃时,该反应的平衡常数为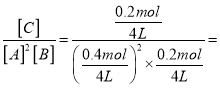 100,故A错误;
100,故A错误;
由图乙可知,升高温度,C的百分含量增大,所以ΔH>0,投料比等于系数比,达到平衡时生成物百分含量最大,故a=2,故B错误 ;根据图甲,200℃时,向容器中加入0.8molA 和0.4molB,达到平街时C的体积分数等于0.25;200℃时,向容器中加入2molA 和1molB,相当于加压,平衡正向移动,达到平街时C的体积分数大于0.25,故C正确;当外界条件由200℃降温到100℃,原平衡一定被破坏,正逆反应速率均减小,故D错误。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】如图所示,两瓶体积相等的气体,在同温同压时瓶内气体(N2O和CO2不发生化学反应)的关系不一定正确的是( ) 
A.所含氧原子数相等
B.气体的总质量相等
C.气体所含电子总数相等
D.气体的密度相等
【题目】[2016江苏][双选]根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A. | 室温下,向苯酚钠溶液中通入足量CO2,溶液变浑浊 | 碳酸的酸性比苯酚的强 |
B. | 室温下,向浓度均为0.1 mol·L1 的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀 | Ksp(BaSO4 )<Ksp(CaSO4) |
C. | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的氧化性比I2的强 |
D. | 室温下,用pH 试纸测得:0.1 mol·L1 Na2SO3溶液的pH约为10;0.1 mol·L1 NaHSO3溶液的pH 约为5 |
|
