��Ŀ����
5��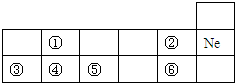 ��ͼ�����ڱ��е�һ���֣�
��ͼ�����ڱ��е�һ���֣���ش��������⣺
��1���ܵ�ԭ�ӽṹʾ��ͼ
 ��
����2���������ڱ��е�λ�õ�3���ڢ�A�壬����Ԫ�ص�������۾�Ϊ+5��
��3���ڢ١���Ԫ���У�ԭ�Ӱ뾶������Al����Ԫ�ط��ţ���ͬ�����õ���������ǿ����F��
��4���ٺ͢ĵ�����һ��������Ӧ���������Ϊ1��4�Ļ�����û������л�ѧ��������Ϊ���ۼ�������Ӽ������ۼ�������
��5���۵ĵ��ʾ���ǿ��ԭ�ԣ���Fe2O3��Ӧ�����ں��Ӹֹ죬д���÷�Ӧ�Ļ�ѧ����ʽ��2Al+Fe2O3$\frac{\underline{\;����\;}}{\;}$Al2O3+2Fe��
���� ��Ԫ�������ڱ���λ�ã���֪��ΪC����ΪF����ΪAl����ΪSi����ΪP����ΪCl��
��1����ΪSi��ԭ�Ӻ�����12�����ӣ���3�����Ӳ㣬���������Ϊ2��8��4��
��2����Ԫ��λ�ÿ�֪����λ�����ڱ��е�3���ڢ�A�壬��������ϼ۵���������������
��3��ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶���縺��Խǿ����õ�������Խǿ��
��4�����ٺ͢ĵ�����һ��������Ӧ���������Ϊ1��4�Ļ�����ΪCCl4��
��5��Al���������������ȷ�Ӧ����Fe����������
��� �⣺��Ԫ�������ڱ���λ�ã���֪��ΪC����ΪF����ΪAl����ΪSi����ΪP����ΪCl��
��1����ΪSi��ԭ�Ӻ�����12�����ӣ���3�����Ӳ㣬���������Ϊ2��8��4��ԭ�ӽṹʾ��ͼΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2����Ԫ��λ�ÿ�֪����λ�����ڱ��е�3���ڢ�A�壬��������ϼ۵����������������ʸ�Ԫ����������ϼ�Ϊ+5���ʴ�Ϊ����3���ڢ�A�壻+5��
��3��ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶��������Ԫ����Al��ԭ�Ӱ뾶�������FԪ�صĵ縺�����F��õ���������ǿ���ʴ�Ϊ��Al��F��
��4�����ٺ͢ĵ�����һ��������Ӧ���������Ϊ1��4�Ļ�����ΪCCl4��Cԭ����Clԭ��֮���γɹ��ۼ����ʴ�Ϊ�����ۼ���
��5��Al���������������ȷ�Ӧ����Fe������������Ӧ����ʽΪ��2Al+Fe2O3$\frac{\underline{\;����\;}}{\;}$Al2O3+2Fe���ʴ�Ϊ��2Al+Fe2O3$\frac{\underline{\;����\;}}{\;}$Al2O3+2Fe��
���� ���⿼��Ԫ�����ڱ���Ԫ��������Ӧ�ã��ѶȲ���ע��Ի���֪ʶ���������գ�

 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�| A�� | 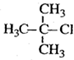 2-��-2-�ȱ��� 2-��-2-�ȱ��� | B�� | 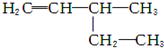 3-�һ�-1-��ϩ 3-�һ�-1-��ϩ | ||
| C�� | 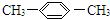 1��4-���ױ� 1��4-���ױ� | D�� | 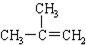 2-����ϩ 2-����ϩ |
�ٱ�ȼ��ʱ��������������Ũ�̵Ļ���
�ڱ����ض��������������������ӳɷ�Ӧ
�۱��������Ը��������Һ����ˮ������Ӧ
�ܱ����Ӿ���ƽ���������νṹ������6��̼ԭ��֮��ļ���ȫ��ͬ��
| A�� | �٢� | B�� | �ڢ� | C�� | �ۢ� | D�� | �٢� |
| A�� | X3YZ4 | B�� | X2YZ3 | C�� | X2YZ4 | D�� | XY2Z3 |

| A�� | �õ�ص�����Ϊп | |
| B�� | �õ�ط�Ӧ�ж���������������� | |
| C�� | ��0.1molZn��ȫ�ܽ�ʱ�������������Һ�ĵ��Ӹ���Ϊ1.204��1023 | |
| D�� | ���������ӦʽΪ��2MnO2+2e-+2H2O�T2MnO��OH��+2OH- |
| A�� | ��ʯ��б��ʯ�����ʯ�����ڹ����ο� | |
| B�� | ���ʯ����Ϊ+2�� | |
| C�� | �������ɳ����������̬������Ϊ����ı��漸��û������ | |
| D�� | б��ʯ����������ʽ�ɱ�ʾΪ��K2O•Al2O3•3SiO2 |
���ڸ����£�����ʯ�뽹̿�Ļ������ͨ��Cl2���õ�TiCl4��һ�ֿ�ȼ���壻
����ϡ�����壨��벣���Χ�ͼ��ȵ������£���þ��TiCl4��Ӧ�ɵõ��ѣ�
����˵������ȷ���ǣ�������
| A�� | ��Ӧ�١��ھ�Ϊ������ԭ��Ӧ | |
| B�� | �ڷ�Ӧ���н��ʯ�ͽ�̿��Ϊ��ԭ�� | |
| C�� | ��Ӧ���п�ȼ��������CO | |
| D�� | ��Ӧ������1molTi����ʱ��ת��4mol e- |
 ������Һ�õ�������ע��Һ�������ǣ���ѧʽΪC6H12O6����ˮ��Һ�����ǩ�ϵIJ���������ͼ��ʾ�����ñ�ǩ��Ϣ���ش��������⣨������ϡ��Һ���ܶ�ԼΪ1g/cm3����
������Һ�õ�������ע��Һ�������ǣ���ѧʽΪC6H12O6����ˮ��Һ�����ǩ�ϵIJ���������ͼ��ʾ�����ñ�ǩ��Ϣ���ش��������⣨������ϡ��Һ���ܶ�ԼΪ1g/cm3����