题目内容
15.(1)写出 CO与氧化铜反应的化学方程式并标明电子转移的方向和数目.CO+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2;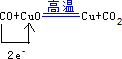 .
.(2)2.8gCO的物质的量为0.1mol,含有1.204×1023个原子,完全与氧化铜反应时失去电子0.2mol.
分析 发生CO+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2,C元素的化合价由+2价升高为+4价,Cu元素的化合价由+2价降低为0,该反应转移2e-,以此来解答.
解答 解:(1)CO与氧化铜反应的化学方程式为CO+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2,C元素的化合价由+2价升高为+4价,Cu元素的化合价由+2价降低为0,该反应转移2e-,电子转移的方向和数目为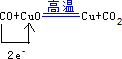 ,故答案为:CO+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2;
,故答案为:CO+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2;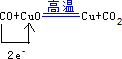 ;
;
(2)2.8gCO的物质的量为$\frac{2.8g}{28g/mol}$=0.1mol,含原子为0.1mol×2×NA=1.204×1023,完全与氧化铜反应时失去电子为0.1mol×(4-2)=0.2mol,
故答案为:0.1;1.204×1023;0.2.
点评 本题考查氧化还原反应,为高频考点,把握氧化还原反应中元素的化合价变化及转移电子为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
5.下列关于化学反应速率的说法正确的是( )
| A. | 化学反应速率是指单位时间内反应物浓度的减少或生成物浓度的增加 | |
| B. | 化学反应速率为“1.0mol/(L.s)”表示的意思是:时间为1s时,某物质的浓度为1.0mol/L | |
| C. | 化学反应速率也有大小也有方向 | |
| D. | 对于任何化学反应来说,反应速率越大,反应现象越明显 |
6.下列变化中一定为放热的化学反应的是( )
| A. | H2O(g)═H2O(l)△H=-44.0 kJ•mol-1 | |
| B. | N2(g)+O2(g)═2NO(g)△H=+182.6 kJ•mol-1 | |
| C. | 形成化学键过程中放出862 kJ热量的化学反应 | |
| D. | 能量变化如图所示的化学反应.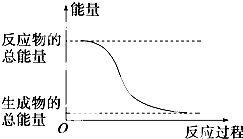 |
3.青少年学生是有知识的人,应懂得“珍爱生命、远离毒品”,以下几种药品或物质中不属于毒品的是( )
| A. | 阿司匹林 | B. | 海洛因 | C. | 大麻 | D. | 鸦片 |
10.能防止贫血的一种元素是( )
| A. | 铁 | B. | 碘 | C. | 铜 | D. | 镁 |
20.ag KNO3溶于bg水,形成VmL饱和溶液.下列关系式错误的是( )
| A. | 该溶液的物质的量浓度:c(KNO3)=$\frac{a}{101V}$mol•L-1 | |
| B. | 该溶液的质量分数:w(KNO3)=$\frac{100a}{a+b}$% | |
| C. | 20℃时KNO3的溶解度S=$\frac{100a}{b}$ g | |
| D. | 该溶液的密度ρ=$\frac{1000(a+b)}{V}$g•L-1 |
7.2005年10月12日我国用长征二号F型火箭成功发射了神舟“六号”载人飞船,并于10月17日圆满着陆.标志着我国载人航天又有新的突破.长征二号F型火箭用的燃料是液态的偏二甲基肼(C2H8N2),氧化剂是液态的N2O4,已知1.5g火箭燃料偏二甲基肼完全燃烧生成氮气,二氧化碳和液态水放出热量50kJ.下列说法不正确的是( )
| A. | 燃料在火箭发动机中燃烧是将化学能主要转变为热能和机械能 | |
| B. | 偏二甲基肼在四氧化氮中的燃烧反应是放热反应 | |
| C. | 该反应中偏二甲基肼和四氧化氮总能量小于二氧化碳、氮气和水的总能量 | |
| D. | 燃烧时的总反应为:C2H8N2+2N2O4$\stackrel{点燃}{→}$2CO2+3N2+4H2O |
4.下列溶液中的Cl浓度与50mL1mol•L-1MgCl2溶液中的Cl-浓度相等的是( )
| A. | 150mL1mol•L-1 NaCl溶液 | B. | 75 mL 0.5mol•L-1 CaCl2溶液 | ||
| C. | 150mL2mol•L-1 KCl溶液 | D. | 75 mL 1 mol•L-1 AlCl3溶液 |