��Ŀ����
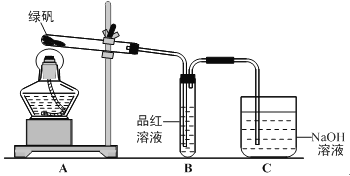
����Ŀ���ò���Fe3����FeSO4��Һ���ò���O2������ˮ���Ƶ�NaOH��Һ��Ӧ�Ʊ���ɫ��Fe(OH)2������
��1������������������������FeSO4��Һʱ�������ϡ�������м����д��������м��ԭ��___________��
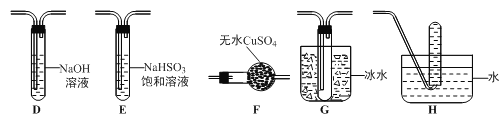
��2����ȥ����ˮ���ܽ��O2�����õķ���___________��
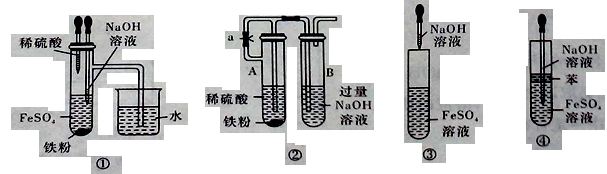
��3�����ɰ�ɫFe ( OH )2�����IJ������ó��ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ���£��ټ���NaOH��Һ�����������������ǣ�_________________��
��4�����и�ͼʾ���ܽϳ�ʱ�俴��Fe ( OH )2��ɫ��������_________(�����)��
���𰸡�
��1����ֹ�������ӱ����������������ӣ���2����У�
��3���������ɵ�Fe( OH )2�����Ӵ�O2����4���٢ڢ� ��
��������
�����������1������FeSO4�����ױ���������ˮ����ص㣬����������Һʱ�������ϡH2SO4��ֹ����ˮ�ⷴӦ��ͬʱ������м��ֹ�����������������ʴ�Ϊ����ֹ�������ӱ�������������������
��2������ˮ��������O2��������Fe(OH)2�����������������ܽ�����¶ȵ����߶���С����˿ɲ��ü�����еķ�����ȥ���ʴ�Ϊ��������У�
��3��Ϊ�������ɵ�Fe(OH)2�����Ӵ�O2�����ó��ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ���£��ټ���NaOH��Һ���ɴﵽĿ�ģ��ʴ�Ϊ���������ɵ�Fe(OH)2�����Ӵ�O2����������
��4����Fe��ϡ���ᷴӦ���ɵ�������װ���ڿ����ų����ɷ�ֹ���ɵ���������������������ѡ����Fe��ϡ���ᷴӦ���ɵ�������װ���ڿ����ų���������������ѹ��ʹ����������NaOH�Ӵ�����Ӧ���ɷ�ֹ���ɵ���������������������ѡ����û�и������������ɵ������������ױ��������ʲ�ѡ�����������������ɷ�ֹ���ɵ���������������������ѡ���ʴ�Ϊ�٢ڢ� ��

 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�