题目内容
4.下列说法正确的是( )| A. | H2O的摩尔质量是18g | |
| B. | 一个12C的实际质量约等于$\frac{12}{6.02×1{0}^{23}}$g | |
| C. | 任何物质的摩尔质量都等于它的式量 | |
| D. | SO2的摩尔质量是64g/mol |
分析 A.单位错误;
B.根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算;
C.摩尔质量和式量在数值上相等;
D.SO2的摩尔质量是64g/mol.
解答 解:A.H2O的摩尔质量是18g/mol,故A错误;
B.由n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$可知一个12C的实际质量约等于$\frac{12}{6.02×1{0}^{23}}$g,故B正确;
C.摩尔质量和式量在数值上相等,但摩尔质量的单位为g/mol,故C错误;
D.SO2的相对分子质量为64,则摩尔质量是64g/mol,故D正确.
故选BD.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握相关计算公式以及单位等问题,难度不大.

练习册系列答案
相关题目
15.在200℃将一定量的O2、CO2和H2O的混合气体经过一定量的碱石灰后,固体质量增加了5.4g,则得到的混合气体(200℃)的平均摩尔质量可能是( )
| A. | 11.5g/mol | B. | 24.3g/mol | C. | 48.4g/mol | D. | 16.2g/mol |
12.利用如图所示装置进行下列实验,能得出相应实验结论是( )
| 选项 | ① | ② | ③ | 实验结论 | 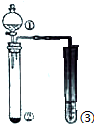 |
| A | 稀硫酸 | KI | AgNO3与AgCl的浊液 | Ksp(AgCl)>Ksp(AgI) | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、强氧化性 | |
| C | 稀盐酸 | Na2SO3 | KMnO4溶液 | SO2有漂白性 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
16.25℃时,在10mL浓度为0.2mol/L NaOH溶液中,滴加0.1mol/L的醋酸,下列有关溶液中粒子浓度关系正确的是( )
| A. | 未加醋酸时:c(OH-)=c(Na+) | |
| B. | 加入10mL醋酸时:c(OH-)>c(Na+)>c(CH3COO-)>c(H+) | |
| C. | 加入醋酸至溶液pH=7时:c(CH3COO-)=c(Na+) | |
| D. | 加入20mL醋酸时:2c(OH-)=c(CH3COO-)+2c(H+) |
4.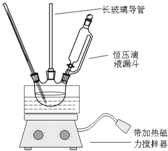 硝基苯是重要的精细化工原料,是医药和染料的中间体制备,还可做有机溶剂.制备硝基苯的过程如下:
硝基苯是重要的精细化工原料,是医药和染料的中间体制备,还可做有机溶剂.制备硝基苯的过程如下:
①配制混酸:组装如图反应装置.取100mL烧杯,用20mL浓硫酸与浓硝酸18mL配制混和酸,加入漏斗中.把18mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀.
③在50-60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品.
已知(1)
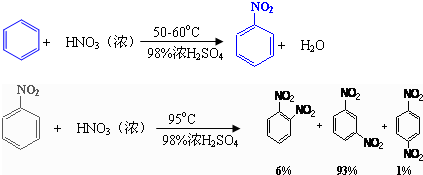
(2)可能用到的有关数据列表如下
请回答下列问题:
(1)配置混酸应先在烧杯中先加入浓硝酸.
(2)恒压滴液漏斗的优点是可以保持漏斗内压强与发生器内压强相等,使漏斗内液体能顺利流下.
(3)实验装置中长玻璃管可用冷凝管(球形冷凝管或直行冷凝管均可)代替(填仪器名称).
(4)反应结束后产品在液体的下层(填“上”或者“下”),分离混酸和产品的操作方法为分液.
(5)用10%Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?取最后一次洗涤液,向溶液中加入氯化钙,无沉淀生成,说明已洗净.
(6)为了得到更纯净的硝基苯,还须先向液体中加入氯化钙除去水,然后蒸馏.
 硝基苯是重要的精细化工原料,是医药和染料的中间体制备,还可做有机溶剂.制备硝基苯的过程如下:
硝基苯是重要的精细化工原料,是医药和染料的中间体制备,还可做有机溶剂.制备硝基苯的过程如下:①配制混酸:组装如图反应装置.取100mL烧杯,用20mL浓硫酸与浓硝酸18mL配制混和酸,加入漏斗中.把18mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀.
③在50-60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品.
已知(1)

(2)可能用到的有关数据列表如下
| 物质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 1,3-二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | / | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | / | 338 | 1.84 | 易溶于水 |
(1)配置混酸应先在烧杯中先加入浓硝酸.
(2)恒压滴液漏斗的优点是可以保持漏斗内压强与发生器内压强相等,使漏斗内液体能顺利流下.
(3)实验装置中长玻璃管可用冷凝管(球形冷凝管或直行冷凝管均可)代替(填仪器名称).
(4)反应结束后产品在液体的下层(填“上”或者“下”),分离混酸和产品的操作方法为分液.
(5)用10%Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?取最后一次洗涤液,向溶液中加入氯化钙,无沉淀生成,说明已洗净.
(6)为了得到更纯净的硝基苯,还须先向液体中加入氯化钙除去水,然后蒸馏.
5.某种兴奋剂的结构简式如图所示,有关该物质说法正确的是 ( )


| A. | 该分子中所有氢原子不可能在同一平面上 | |
| B. | 1mol该物质与氢气反应,最多消耗4mol氢气 | |
| C. | 加入FeCl3溶液呈紫色,因为该物质含有酚类结构特征 | |
| D. | 滴入酸性高锰酸钾溶液,紫色褪去,可证明结构存在碳碳双键 |