题目内容
【题目】Ⅰ.从固体混合物A出发可以发生如下框图所示的一系列变化。
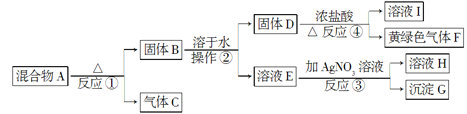
G为不溶于稀硝酸的白色固体,溶液H的焰色反应呈紫色(透过蓝色的钴玻璃观察)。
回答下列问题:
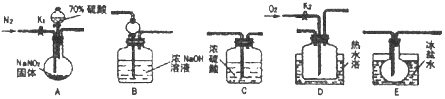
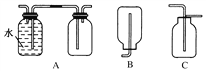
(1)在实验室中收集气体C,可选择如图(左下)装置中的__________________________
(2)操作②的名称是_______________
(3)写出反应④的离子方程式:___________________________________________________
(4)写出反应的化学方程式:___________________________________________________
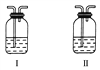
(5)在实验室中,要获得干燥纯净的黄绿色气体F,可以将它依次通过如上图中的Ⅰ、Ⅱ装置,其中瓶Ⅰ中盛放的是_________________,瓶Ⅱ中盛放的是_____________________
Ⅱ.如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。

现欲用该浓硫酸配制成1mol/L的稀硫酸。
现实验室仅需要这种稀硫酸220mL.试回答下列问题:
(1)用量筒量取该浓硫酸 ________mL。
(2)配制时,必须使用的仪器除量筒、烧杯、玻璃棒、胶头滴管外,还缺少的玻璃仪器是__________________。
(3)配制溶液的过程中,其他操作都正确,
下列操作会使所配溶液浓度偏高的是_________。
A.用量筒量取浓硫酸时俯视
B.稀释浓硫酸时,未冷却到室温即转移到容量瓶中
C.量取浓H2SO4后的量筒进行洗涤,并将洗涤液转移到容量瓶中。
D.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至凹液面最低处与刻度线相切
E.容量瓶不干燥
F.定容时,俯视容量瓶刻度线
【答案】 AC 过滤 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 2KClO3
Mn2++Cl2↑+2H2O 2KClO3![]() 2KCl+3O2↑ 饱和食盐水 浓硫酸 13.6 250mL容量瓶 BCF
2KCl+3O2↑ 饱和食盐水 浓硫酸 13.6 250mL容量瓶 BCF
【解析】试题分析:本题以KClO3与MnO2混合加热制备O2为基础、主要考查氧气的收集方法、固体与液体的分离操作方法、O2和Cl2制备反应原理、Cl2的除杂方法、物质的量浓度与质量分数的换算、配置一定物质的量浓度的溶液等基础知识,考查考生对物质变化流程图的认知和分析能力、实验设计能力、配置一定物质的量浓度溶液实验的总体掌握程度。
解析:Ⅰ、D与浓盐酸反应生成的黄绿色气体F是Cl2,反应物固体D难溶于水只能是MnO2,则溶液I的溶质是MnCl2。溶液E加入AgNO3生成的不溶于稀硝酸的白色沉淀G是AgCl,溶液H的焰色反应说明H是钾的化合物,应该是KNO3,则E是KCl,所以固体B是MnO2与KCl的混合物。混合物A加热反应后留下固体混合物MnO2和KCl,所以A是KClO3与MnO2的混合物,加热后得到的气体C是O2。(1)O2的密度大于空气且难溶于水,所以收集O2采用向上排空气法或者排水法,结合本题图示应当选择A或者C。正确答案:AC。操作②是分离KCl和MnO2的固体混合物,由于KCl易溶于水而MnO2不溶于水,所以混合物溶于水后可以采用过滤的方法进行分离。正确答案:过滤。(3)反应④是MnO2与浓HCl反应制备Cl2,反应离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O。正确答案:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O。正确答案:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O。(4)反应①是KClO3与MnO2加热制O2,反应原理是2KClO3
Mn2++Cl2↑+2H2O。(4)反应①是KClO3与MnO2加热制O2,反应原理是2KClO3![]() 2KCl+3O2↑。正确答案:2KClO3
2KCl+3O2↑。正确答案:2KClO3![]() 2KCl+3O2↑。(5)上述制得的Cl2中含有HCl和水蒸气,可以先通过饱和食盐水除去HCl气体,再通过浓硫酸干燥除去水蒸气。正确答案:饱和食盐水、浓硫酸。Ⅱ、98%的浓硫酸浓度
2KCl+3O2↑。(5)上述制得的Cl2中含有HCl和水蒸气,可以先通过饱和食盐水除去HCl气体,再通过浓硫酸干燥除去水蒸气。正确答案:饱和食盐水、浓硫酸。Ⅱ、98%的浓硫酸浓度![]() 。(1)根据常用容量瓶的规格,仅需要220mL溶液时,需要配制250mL溶液,配制稀硫酸过程中溶质H2SO4保持不变,则C1V1=C2V2,既18.4mol/L×V1=1mol/L×0.250L,V1=0.0136L=13.6mL。正确答案:13.6mL。(2)配制时需要使用的玻璃仪器包括:250mL容量瓶、量筒、烧杯、玻璃棒、胶头滴管,因此缺少的玻璃仪器是250mL容量瓶。正确答案:250mL容量瓶。(3)A、用量筒量取浓硫酸时俯视,则读取13.6mL时实际浓硫酸体积偏少,所配制溶液浓度偏小,A错误。B、稀释浓硫酸时未冷却到室温将导致溶液热膨胀体积增大,所以定容到250mL时,冷却后的溶液体积不到250mL,所配制溶液浓度偏大,B正确。C、量筒标记体积刻度时并不考虑倾倒后残留液体,所以量取浓H2SO4后的量筒进行洗涤将会使得溶质硫酸增加,所配制溶液浓度偏大,C正确。D、定容后的浓度应该是正确的浓度,后又加入蒸馏水会使溶液变稀,浓度变小,D错误。E、容量瓶中本身存在的水不影响稀溶液的浓度,E错误。F、定容时俯视容量瓶刻度线将导致实际体积偏小,所配制溶液浓度偏大,F正确。正确答案BCF。
。(1)根据常用容量瓶的规格,仅需要220mL溶液时,需要配制250mL溶液,配制稀硫酸过程中溶质H2SO4保持不变,则C1V1=C2V2,既18.4mol/L×V1=1mol/L×0.250L,V1=0.0136L=13.6mL。正确答案:13.6mL。(2)配制时需要使用的玻璃仪器包括:250mL容量瓶、量筒、烧杯、玻璃棒、胶头滴管,因此缺少的玻璃仪器是250mL容量瓶。正确答案:250mL容量瓶。(3)A、用量筒量取浓硫酸时俯视,则读取13.6mL时实际浓硫酸体积偏少,所配制溶液浓度偏小,A错误。B、稀释浓硫酸时未冷却到室温将导致溶液热膨胀体积增大,所以定容到250mL时,冷却后的溶液体积不到250mL,所配制溶液浓度偏大,B正确。C、量筒标记体积刻度时并不考虑倾倒后残留液体,所以量取浓H2SO4后的量筒进行洗涤将会使得溶质硫酸增加,所配制溶液浓度偏大,C正确。D、定容后的浓度应该是正确的浓度,后又加入蒸馏水会使溶液变稀,浓度变小,D错误。E、容量瓶中本身存在的水不影响稀溶液的浓度,E错误。F、定容时俯视容量瓶刻度线将导致实际体积偏小,所配制溶液浓度偏大,F正确。正确答案BCF。

【题目】A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示。
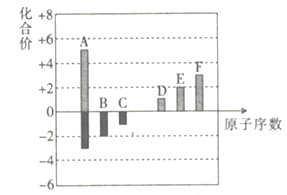
(1)将A、E两种元素的元素符号填入下表中正确的位置上。________
族序数 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ||||||||
二 | ||||||||
三 | ||||||||
(2)A、B、C、D、E、F六种元素中非金属性最强的是____________(填元素符号),B、D两元素可以组成原子个数比为1:1的离子化合物,写出该离子化合物的电子式:______,A、B两元素对应的气态氢化物的稳定性强弱关系是________________(用化学式表示)。
(3)写出D、F两元素的最高价氧化物对应的水化物反应的离子方程式:________________________