题目内容
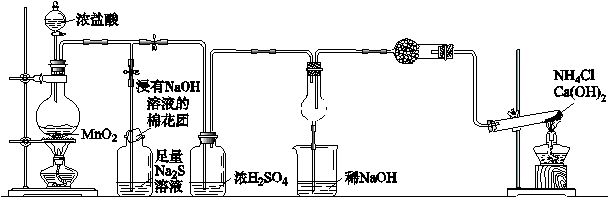
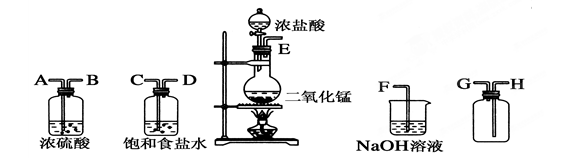
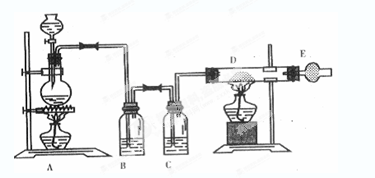
某化学小组为了证明SO2和Cl2的漂白性,设计了如下图所示的实验装置:
它们制备SO2和Cl2所依据的原理分别是:
Na2SO3+H2SO4= Na2SO4+H2O+SO2↑ MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)用来制取Cl2的装置是 (填序号),反应中浓盐酸所表现出的化学性质是 和
(2)反应开始一段时间后, B、D试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,____ __ (填“B”或“D” )试管中无明显现象。
(3)装置C的作用是 ;
(4) 若装置D中的品红溶液换成紫色的石蕊溶液,则出现的现象是 。
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是 。
(1) E;还原性、酸性;(2) D ;(3)吸收多余的SO2和Cl2;(4)先变红,后褪色;
(5)SO2+Cl2+2H2O ==2HCl+H2SO4。
解析试题分析:(1)根据反应物的状态和反应条件选择反应装置,根据题给信息知,实验室制取氯气所用药品是固体和液体,反应条件是加热,所以应选用固液加热型装置,选E;实验室制取氯气的反应方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,由HCl生成MnCl2,氯元素化合价不变,由HCl生成Cl2,氯元素化合价降低,所以浓盐酸所表现出的性质是酸性和还原性;(2)氯气通入品红溶液中红色褪去,是利用次氯酸的强氧化性,生成的无色物质稳定,加热不复原;二氧化硫的漂白性是利用二氧化硫和有色物质化合生成无色物质,生成的无色物质不稳定,加热复原;选D;(3)氯气和二氧化硫有毒不能直接排空,需进行尾气处理,装置C的作用是吸收多余的SO2和Cl2;(4) 若装置D中的品红溶液换成紫色的石蕊溶液,则出现的现象是先变红,后褪色;氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,离子反应方程式为:Cl2+2OH-=Cl-+ClO-+H2O,二氧化硫和氢氧化钠反应生成盐和水,离子方程式为:SO2+2OH-=SO32-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;SO2+2OH-=SO32-+H2O;(5)氯气有强氧化性,二氧化硫有还原性,二者能按1:1发生氧化还原反应生成盐酸和硫酸而使气体失去漂白性,反应方程式为Cl2+SO2+2H2O=H2SO4+2HCl。
MnCl2+Cl2↑+2H2O,由HCl生成MnCl2,氯元素化合价不变,由HCl生成Cl2,氯元素化合价降低,所以浓盐酸所表现出的性质是酸性和还原性;(2)氯气通入品红溶液中红色褪去,是利用次氯酸的强氧化性,生成的无色物质稳定,加热不复原;二氧化硫的漂白性是利用二氧化硫和有色物质化合生成无色物质,生成的无色物质不稳定,加热复原;选D;(3)氯气和二氧化硫有毒不能直接排空,需进行尾气处理,装置C的作用是吸收多余的SO2和Cl2;(4) 若装置D中的品红溶液换成紫色的石蕊溶液,则出现的现象是先变红,后褪色;氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,离子反应方程式为:Cl2+2OH-=Cl-+ClO-+H2O,二氧化硫和氢氧化钠反应生成盐和水,离子方程式为:SO2+2OH-=SO32-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;SO2+2OH-=SO32-+H2O;(5)氯气有强氧化性,二氧化硫有还原性,二者能按1:1发生氧化还原反应生成盐酸和硫酸而使气体失去漂白性,反应方程式为Cl2+SO2+2H2O=H2SO4+2HCl。
考点:考查氯气和二氧化硫的制备和性质。

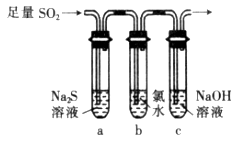
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得。已知:Na2S2O3在酸性溶液中不能稳定存在。
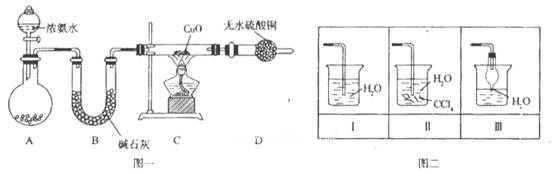
(1)某研究小组设计的制备Na2S2O3·5H2O的装置和部分操作步骤如下。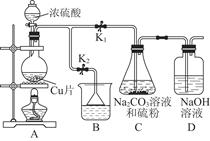
Ⅰ.打开K1关闭K2,向圆底烧瓶中加入足量浓硫酸,加热。
Ⅱ.C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少,当C中溶液的pH 接近7时,打开K2,关闭K1即停止C中的反应,停止加热。
Ⅲ.过滤C中的混合液。
Ⅳ.将滤液经过 、 、过滤、洗涤、烘干,得到产品Na2S2O3·5H2O。
①Ⅱ中,“当C中溶液的pH接近7时即停止C中的反应”的原因是 (用离子方程式表示)。
②Ⅳ中,操作步骤是 、 。
③装置B中盛放的试剂是(填化学式) 溶液。
④有一小组在实验中发现,二氧化硫气体产生缓慢以致后续现象不明显,但又不存在气密性问题,请你推测可能的原因 。
(2)常用Na2S2O3溶液测定废水中Ba2+的浓度,步骤如下:取废水25.00 mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过KI溶液,充分反应后得混合溶液V mL,将其平均分成4等份,加入淀粉溶液作指示剂,用0.001 0 mol·L-1的Na2S2O3溶液进行滴定,反应完全时,相关数据记录如下表所示:
| 编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准 | | | | |
| 溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
部分反应离子方程式为:
①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;
②I2+2S2O32-=2I-+S4O62-。
则判断达到滴定终点的现象是 ,废水中Ba2+的物质的量浓度 _。
请分析回答某同学在探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铜反应的实验中发现的有关问题。
Ⅰ.探究上述四种酸的氧化性相对强弱及其与铜反应的还原产物的性质
(1)分别向盛有等量铜片的四支试管中加入等体积的浓硫酸、稀硫酸、浓硝酸、稀硝酸,实验结果记录如下表:
| | 酸 | 实验结果 |
| a | 浓硫酸 | 加热后发生反应,产生无色刺激性气体 |
| b | 稀硫酸 | 加热也不发生反应 |
| c | 浓硝酸 | 不加热即发生反应,产生红棕色气体 |
| d | 稀硝酸 | 微热发生反应,产生无色气体 |
①由上表中实验结果,四种酸的氧化性由强到弱的顺序是 。
②由上表可知,铜与稀硫酸在加热条件下不反应,但若同时通入O2,铜片能逐渐溶解,溶液变为蓝色。写出该反应的化学方程式:
(2)先将铜与浓硫酸反应产生的气体X持续通入如图所示装置中,一段时间后再将铜与浓硝酸产生的气体Y也持续通入该装置中,则整个过程中可观察到的现象包括 (填字母)。

A.通入X气体后产生白色沉淀
B.通入X气体后溶液无明显现象
C.通入Y气体后产生沉淀
D.通入Y气体后沉淀溶解
E.通入Y气体后溶液中无明显现象
由此可得到的结论是 (填字母)。
A.硝酸的酸性比硫酸强
B.H2SO3的酸性比盐酸强
C.HNO3能氧化H2SO3(或SO2)
D.BaSO4既不溶于水也不溶于HNO3溶液
Ⅱ.如图是某同学探究铜与稀硝酸反应的还原产物的实验装置图,请回答下列问题:

(1)写出铜与稀硝酸反应的离子方程式: 。
(2)已知装置气密性良好,请简述利用该装置证明铜与稀硝酸反应生成的气体产物是NO的操作过程: