题目内容
5.下列电离方程式错误的是( )| A. | CH3COOH→H++CH3COO- | B. | NaHCO3→Na++HCO3- | ||
| C. | NH4Cl→NH4++Cl- | D. | H2S  H++HS- H++HS- |
分析 A.醋酸为弱电解质,部分电离,用可逆符号;
B.碳酸氢钠为强电解质,完全电离;
C.氯化铵为强电解质,完全电离;
D.硫化氢为多元弱酸,分步电离,以第一步为主.
解答 解:A.醋酸为弱电解质,部分电离,电离方程式:CH3COOH  H++CH3COO-,故A错误;
H++CH3COO-,故A错误;
B.碳酸氢钠为强电解质,完全电离,电离方程式:NaHCO3=Na++HCO3-,故B正确;
C.氯化铵为强电解质,完全电离,电离方程式:NH4Cl=NH4++Cl-,故C正确;
D.硫化氢为多元弱酸,分步电离,以第一步为主,电离方程式:H2S  H++HS-,故D正确;
H++HS-,故D正确;
故选:A.
点评 本题考查了电解质电离方程式的书写明确电解质强弱及电离方式是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.对下列装置或操作描述正确的是( )


| A. | 图①用于实验室制乙烯 | |
| B. | 图②用于实验室制乙炔并验证乙炔可以发生氧化反应 | |
| C. | 图③用于实验室中分馏石油 | |
| D. | 图④中若A为醋酸,B为贝壳,C为苯酚钠溶液,则可验证醋酸的酸性大于碳酸,但不能验证碳酸的酸性大于苯酚 |
16.下列说法中正确的是( )
| A. | 互为同分异构体的物质具有相同的分子式 | |
| B. | 同系物的分子中各元素的原子个数比都相同 | |
| C. | 含元素种类相同而结构不同的化合物互称为同分异构体 | |
| D. | 具有相同通式,分子组成相差若干个-CH2原子团的有机物互称同系物 |
13.下列各组物质中符合“酸、碱、盐、酸性氧化物”顺序的是( )
| A. | H2SO4、Na2O、MgCl2、CO2 | B. | NaHCO3、Ba(OH)2、Na2CO3、ZnO | ||
| C. | HNO3、Ca(OH)2、Na2CO3、SO3 | D. | HCl、KOH、Na2CO3、MgO |
20.已知烯烃经臭氧氧化后,在Zn存在下水解,可得醛或酮.如: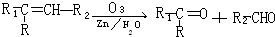 ,现有化学式为C10H20的烯烃,它经臭氧氧化后在Zn存在下水解只生成一种有机物.符合该条件的结构共有( )
,现有化学式为C10H20的烯烃,它经臭氧氧化后在Zn存在下水解只生成一种有机物.符合该条件的结构共有( )
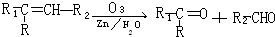 ,现有化学式为C10H20的烯烃,它经臭氧氧化后在Zn存在下水解只生成一种有机物.符合该条件的结构共有( )
,现有化学式为C10H20的烯烃,它经臭氧氧化后在Zn存在下水解只生成一种有机物.符合该条件的结构共有( )| A. | 7种 | B. | 6种 | C. | 5种 | D. | 4种 |
10.利用右图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 浓盐酸 | MnO2 | NaOH | 制氯气并吸收尾气 | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
16.将250mL含BaCl2和KCl的混合溶液分成5等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀.则原混合溶液中钾离子物质的量浓度为
( )
( )
| A. | 4(b-2a)mol/L | B. | 20(2a-b)mol/L | C. | 20(b-2a)mol/L | D. | 10(b-a)mol/L |
13.若溶液中由水电离产生的C(OH-)=1×10-14 mol•L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
| A. | Al3+ Na+ NO3- Cl- | B. | K+ Na+ Cl- NO3- | ||
| C. | K+ Na+ Cl- AlO2- | D. | K+ NH4+ SO42- NO3- |
12.已知X、Y、Z为三种可溶性盐,其阳离子分别是Cu2+、Ag+、Na+中的一种,阴离子分别是SO42-、NO3-、CO32-中的一种(离子在物质中不能重复出现).现设计以下实验:
部分物质的溶解性
①将三种盐分别溶于盛有蒸馏水的三支试管中,只有Z的溶液呈蓝色;
②向①的三支试管中分别加入稀盐酸,发现X的溶液中产生白色沉淀,Y的溶液中有无色无味的气体逸出.
根据①②实验现象回答下列问题:
(1)写出X、Y、Z的化学式:XAgN03 YNa2CO3 ZCuSO4
(2)写出稀盐酸与X反应的离子方程式Ag++Cl-═AgCl↓.
(3)写出Z与Ba(OH)2溶液反应的离子方程式Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓.
部分物质的溶解性
| NO3- | SO42- | CO32- | |
| Na+ | 溶 | 溶 | 溶 |
| Cu2+ | 溶 | 溶 | - |
| Ag+ | 溶 | 微 | 不 |
②向①的三支试管中分别加入稀盐酸,发现X的溶液中产生白色沉淀,Y的溶液中有无色无味的气体逸出.
根据①②实验现象回答下列问题:
(1)写出X、Y、Z的化学式:XAgN03 YNa2CO3 ZCuSO4
(2)写出稀盐酸与X反应的离子方程式Ag++Cl-═AgCl↓.
(3)写出Z与Ba(OH)2溶液反应的离子方程式Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓.