题目内容
【题目】A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
(1)当n=2时,写出AB2的电子式______________,分子中有______________个σ键,______________个π键。
(2)当n=3时,A单质形成的晶体属于______________晶体;
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是______________(用元素符号表示)。
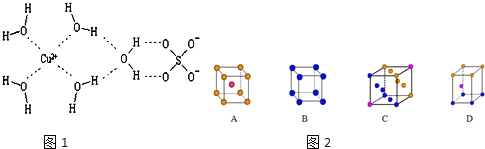
(4)已知某红紫色络合物的组成为CoCl35NH3H2O。该络合物中的中心离子钴离子在基态时核外电子排布简式为______________;
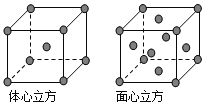
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为______________。
【答案】(1)![]() ;
;
(2)原子;
(3)P>S>Si;
(4)1s22s22p63s23p63d6(或[Ar]3d6);
(5)1:2
【解析】试题分析:A、B、C、D为前四周期元素,B元素的最外层电子数是其电子层数的3倍,最外层电子数不超过8个,所以该元素为O元素,C元素原子的M电子层的P亚层中有3个未成对电子,则C是P元素,D元素原子核外的N层中只有2对成对电子,则D的核外电子排布式为:1s22s22p63s23p4,则D是S元素。
(1)当n=2时,A元素的原子价电子排布为ns2np2,则A为C元素,AB2为CO2,其电子式为![]() ,二氧化碳中碳氧之间是双键,其中有一个是σ键,一个是π键,所以每个二氧化学碳中含有2个σ键和2个π键,故答案为:
,二氧化碳中碳氧之间是双键,其中有一个是σ键,一个是π键,所以每个二氧化学碳中含有2个σ键和2个π键,故答案为:![]() ;
;
(2)当n=3时,A元素的原子价电子排布为ns2np2,则A为Si元素,A单质形成的晶体属于原子晶体,故答案为:原子;
(3)若A元素的原子价电子排布为3s23p2,则A为Si元素,同周期元素从左向右,第一电离能增大,但Si、P、S三种元素中,由于P元素的最外层电子处于半满状态,是一种稳定结构,其第一电离能高于同周期相邻的元素,所以Si、P、S的第一电离能由大到小的顺序是P>S>Si,故答案为:P>S>Si;
(4)钴离子的化合价是+3价,钴离子核外有24个电子,其基态时核外电子排布式为1s22s22p63s23p63d6,故答案为:1s22s22p63s23p63d6(或[Ar]3d6);
(5)体心立方晶胞中含有Fe原子的个数为8×![]() +1=2,面心立方晶胞中实际含有的Fe原子个数为8×
+1=2,面心立方晶胞中实际含有的Fe原子个数为8×![]() +6×
+6×![]() =4,所以体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为1:2,故答案为:1:2。
=4,所以体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为1:2,故答案为:1:2。

 出彩同步大试卷系列答案
出彩同步大试卷系列答案