题目内容
【题目】氨水和盐酸是常见的化学试剂,可将氨气(NH3)、氯化氢气体分别溶于水制得. 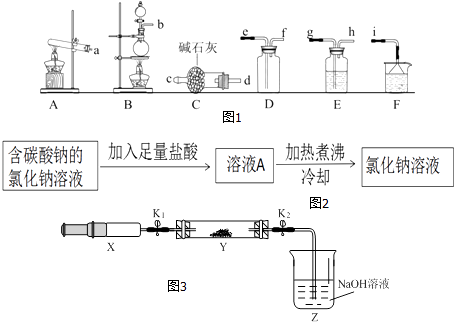
(1)氨气的发生装置可以选择如图1中的 , 反应的化学方程式为 .
(2)欲收集一瓶干燥的氨气,选择如图中的装置,其连接顺序为:发生装置→(按气流方向,用小写字母表示).
(3)小华为探究氨气溶于水是否发生化学反应,设计并完成如表实验(填写表中空白):
实验操作 | 实验现象及结论 |
将浸有酚酞溶液的滤纸干燥后,放入盛有干燥氨气的集气瓶中 | 无明显现象 |
(4)小明将滴有酚酞的稀氨水加热,观察到溶液颜色变浅,原因可能是 .
(5)小芳将滴有石蕊的稀盐酸加热,溶液颜色无明显变化.为进一步研究,取稀盐酸分成2份:①未经加热;②加热煮沸一段时间后冷却,分别中和等量的氢氧化钠,消耗二者的质量:①>②,则稀盐酸经加热煮沸后浓度(填“增大”、“减小”或“不变”).为除去氯化钠溶液中的碳酸钠,小林设计了如图2方案:
你认为上述方案(填“合理”或“不合理”),请分析:(如合理,说明原因;如不合理,说明原因并设计改进方案).
(6)为研究氨气的还原性,小兰做了一下实验:
将(2)收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好).在一定温度如图3所示装置进行实验.
操作步骤 | 实验现象 | 解释原因 |
打开K1 , 推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中 | ②反应的化学方程式 |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
打开K2 | ③ | ④ |
【答案】
(1)A或B;2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O或NH3?H2O
CaCl2+2NH3↑+2H2O或NH3?H2O ![]() NH3↑+H2O
NH3↑+H2O
(2)d→c→f→e→i
(3)将浸有酚酞溶液的滤纸湿润后,放入盛有干操氨气的集气瓶中;滤纸变红,说明氨气遇水形成溶液呈碱性
(4)氨水不稳定受热易分解生成氨气和水,导致溶液碱性减弱,则溶液颜色变浅
(5)增大;不合理;根据上述实验,加热煮沸无法除去溶液A中混有的过量氯化氢.改进方案:向含碳酸钠的氯化钠溶液中边逐滴加盐酸,边测定溶液的pH,至溶液呈中性即可
(6)红棕色气体慢慢变浅,最后褪为无色;8NH3+6NO2 ![]() 7N2+12H2O;Z中的NaOH溶液倒吸入Y管中;该反应是气体体积减小的反应,Y管内压强降低,在大气压的作用下发生倒吸
7N2+12H2O;Z中的NaOH溶液倒吸入Y管中;该反应是气体体积减小的反应,Y管内压强降低,在大气压的作用下发生倒吸
【解析】解:(1.)实验室制备氨气,可以利用氯化铵和氢氧化钙固体加热反应生成,选择装置A进行,反应的化学方程式为:2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O,也可以利用浓氨水滴入固体氧化钙或氢氧化钠或碱石灰中利用溶解放热时一水合氨分解生成,反应的化学方程式为:NH3H2O
CaCl2+2NH3↑+2H2O,也可以利用浓氨水滴入固体氧化钙或氢氧化钠或碱石灰中利用溶解放热时一水合氨分解生成,反应的化学方程式为:NH3H2O ![]() NH3↑+H2O,所以答案是:A或B,2NH4Cl+Ca(OH)2
NH3↑+H2O,所以答案是:A或B,2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O,NH3H2O
CaCl2+2NH3↑+2H2O,NH3H2O ![]() NH3↑+H2O.
NH3↑+H2O.
(2.)欲收集一瓶干燥的氨气,需要发生装置制备出氨气,通过碱石灰吸收水蒸气,通过向上排气法收集,剩余氨气需要吸收防倒吸,选择装置连接为:发生装置→d→c→f→e→i,
所以答案是:d→c→f→e→i;
(3.)将浸有酚酞溶液的滤纸湿润后,放入盛有干操氨气的集气瓶中,滤纸变红,说明氨气遇水溶液呈碱性,所以答案是:
实验操作 | 实验现象及结论 |
将浸有酚酞溶液的滤纸湿润后,放入盛有干操氨气的集气瓶中 | 滤纸变红,说明氨气遇水形成溶液呈碱性 |
(4.)小明将滴有酚酞的稀氨水加热,观察到溶液红色变浅,原因可能是氨水不稳定受热易分解生成氨气和水,导致溶液碱性减弱,则溶液颜色变浅,所以答案是:氨水不稳定受热易分解生成氨气和水,导致溶液碱性减弱,则溶液颜色变浅;
(5.)取稀盐酸分成2份:①未经加热;②加热煮沸一段时间后冷却,分别中和等量的氢氧化钠,消耗二者的量:①>②,因为中和等量的氢氧化钠,未经加热的溶液用量比加热煮沸后的多,故加热煮沸后稀盐酸浓度增大;碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,所以加入稀盐酸可把碳酸钠转化为氯化钠而除去;根据上述实验,加热煮沸无法除去溶液A中混有的过量HCl;向含有碳酸钠的氯化钠溶液中边逐滴加盐酸,边测定溶液的PH至溶液呈中性即可,或将溶液加入过量的盐酸,再将溶液蒸干,然后重新配制成氯化钠溶液.故不合理.所以答案是:增大;不合理根据上述实验,加热煮沸无法除去溶液A中混有的过量氯化氢.改进方案:向含碳酸钠的氯化钠溶液中边逐滴加盐酸,边测定溶液的pH,至溶液呈中性即可;
(6.)将(2)收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2 , 打开K1 , 推动注射器活塞,使X中的气体缓慢充入Y管中,二氧化氮和氨气发生氧化还原反应生成氮气和水,反应的化学方程式为:8NH3+6NO2 ![]() 7N2+12H2O,红棕色气体颜色变浅,最后褪为无色,打开K2Z中的NaOH溶液倒吸入Y管中,该反应是气体体积减小的反应,Y管内压强降低,在大气压的作用下发生倒吸,
7N2+12H2O,红棕色气体颜色变浅,最后褪为无色,打开K2Z中的NaOH溶液倒吸入Y管中,该反应是气体体积减小的反应,Y管内压强降低,在大气压的作用下发生倒吸,
所以答案是:
操作步骤 | 实验现象 | 解释原因 |
①Y管中红棕色气体慢慢变浅,最后褪为无色 | ②反应的化学方程式8NH3+6NO2 | |
③Z中的NaOH溶液倒吸入Y管中 | ④该反应是气体体积减小的反应,Y管内压强降低,在大气压的作用下发生倒吸 |