题目内容
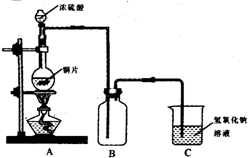
某同学为了检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,选用了下图所示实验装置.
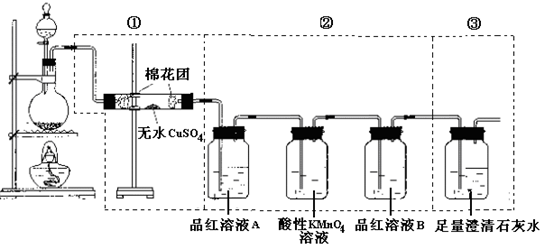
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式______.
(2)①中无水硫酸铜的作用是______.
(3)②中酸性KMnO4溶液的作用是______.
(4)②中两次用到品红溶液,它们的作用分别是A______、B______.
(5)③中出现的现象是______,发生反应的离子方程式是______.

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式______.
(2)①中无水硫酸铜的作用是______.
(3)②中酸性KMnO4溶液的作用是______.
(4)②中两次用到品红溶液,它们的作用分别是A______、B______.
(5)③中出现的现象是______,发生反应的离子方程式是______.
(1)木炭粉与浓硫酸反应,表现了浓硫酸的强氧化性把碳氧化为最高价二氧化碳,本身被还原为二氧化硫,反应生成SO2和CO2,化学方程式为:C+2H2SO4(浓)
2S02↑+C02↑+2H2O,故答案为:C+2H2SO4(浓)
2S02↑+C02↑+2H2O
(2)一般检验含有水汽的混合气体,水通常是第一个检验的;实验利用白色硫酸铜遇到水变为蓝色证明含有水蒸气,①中无水硫酸铜的作用是检验反应生成的水蒸气;
故答案为:检验反应生成的水蒸气;
(3)因S02和C02都能使石灰水变浑浊,因此要想检验出C02,就要先把S02检验了,并除掉S02,这样石灰水变浑浊才能说明有C02,即②一定要在③的前面.根据检验SO2和CO2时,就要先把SO2检验了,并除掉SO2,这样石灰水变浑浊才能说明有CO2,所以高锰酸钾溶液是吸收二氧化硫的作用,故答案为:除去混合气体中的SO2;
(4))根据检验SO2和CO2时,就要先把SO2检验了,并除掉SO2,这样石灰水变浑浊才能说明有CO2,所以②中两次用到品红溶液,它们的作用分别是检验生成的SO2气体;检验SO2是否除尽;故答案为:检验生成的SO2气体;检验SO2是否除尽;
(5)③装置是验证二氧化硫气体除净后,检验二氧化碳气体存在的实验装置,反应现象是二氧化碳和氢氧化钙反应生成白色沉淀;反应的离子方程式为:CO2+Ca2++2OH-=CaCO3↓+H2O;
故答案为:出现白色沉淀; CO2+Ca2++2OH-=CaCO3↓+H2O;
| ||
| ||
(2)一般检验含有水汽的混合气体,水通常是第一个检验的;实验利用白色硫酸铜遇到水变为蓝色证明含有水蒸气,①中无水硫酸铜的作用是检验反应生成的水蒸气;
故答案为:检验反应生成的水蒸气;
(3)因S02和C02都能使石灰水变浑浊,因此要想检验出C02,就要先把S02检验了,并除掉S02,这样石灰水变浑浊才能说明有C02,即②一定要在③的前面.根据检验SO2和CO2时,就要先把SO2检验了,并除掉SO2,这样石灰水变浑浊才能说明有CO2,所以高锰酸钾溶液是吸收二氧化硫的作用,故答案为:除去混合气体中的SO2;
(4))根据检验SO2和CO2时,就要先把SO2检验了,并除掉SO2,这样石灰水变浑浊才能说明有CO2,所以②中两次用到品红溶液,它们的作用分别是检验生成的SO2气体;检验SO2是否除尽;故答案为:检验生成的SO2气体;检验SO2是否除尽;
(5)③装置是验证二氧化硫气体除净后,检验二氧化碳气体存在的实验装置,反应现象是二氧化碳和氢氧化钙反应生成白色沉淀;反应的离子方程式为:CO2+Ca2++2OH-=CaCO3↓+H2O;
故答案为:出现白色沉淀; CO2+Ca2++2OH-=CaCO3↓+H2O;

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目