题目内容
【题目】如表陈述Ⅰ、Ⅱ均正确,且两者在反应原理上相似的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 将 |
|
B |
|
|
C | 玻璃试剂瓶可用于盛放氢氟酸 | 石英坩埚不能用于熔化NaOH |
D |
|
|
A.AB.BC.CD.D
【答案】D
【解析】
A. ![]() 通入
通入![]() 溶液中不反应,将
溶液中不反应,将![]() 气体通入
气体通入![]() 溶液,发生氧化还原反应生成
溶液,发生氧化还原反应生成![]() 沉淀,故A错误;
沉淀,故A错误;
B. 氨气属于碱性气体,能被浓硫酸吸收,所以不能被浓硫酸干燥,![]() 具有较强还原性,能够被浓硫酸氧化,不可以用浓硫酸干燥,故B错误;
具有较强还原性,能够被浓硫酸氧化,不可以用浓硫酸干燥,故B错误;
C. 二氧化硅能与氢氟酸反应:![]() ,氢氟酸应保存在塑料瓶中,二氧化硅能和强碱反应
,氢氟酸应保存在塑料瓶中,二氧化硅能和强碱反应![]() ,石英坩埚不能用于熔化NaOH,故C错误;
,石英坩埚不能用于熔化NaOH,故C错误;
D. ![]() 与水反应,离子方程式为:
与水反应,离子方程式为:![]() ,
,![]() 可与水反应
可与水反应![]() ,均发生氧化还原反应,且既做氧化剂又做还原剂,故D正确;
,均发生氧化还原反应,且既做氧化剂又做还原剂,故D正确;
答案选D。

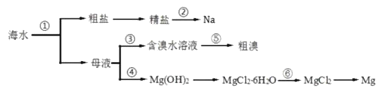
【题目】利用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等.
②沉淀I中只含有两种沉淀。
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中Co2O3发生反应的离子反应方程式为___________。
(2)NaClO3在浸出液中发生的离子反应方程式为_________________。
(3)加入Na2CO3调PH至5.2,目的是__________________________;萃取剂层含锰元素,则沉淀II的主要成分为_____________。
(4)操作I包括:将水层加入浓盐酸调整PH为2~3,___________、____________、过滤、洗涤、减压烘干等过程。
(5)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中CoCl2·6H2O质量分数大于100%,其原因可能是____________________(回答一条原因即可)。
(6)将5.49g草酸钴晶体(CoC2O4·2H2O)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表.
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
经测定,整个受热过程,只产生水蒸气和CO2气体,则290~320℃温度范围,剩余的固体物质化学式为__。
[已知: CoC2O4·2H2O的摩尔质量为183g·mol-1]
【题目】Ⅰ.查阅资料,乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸。
(1)已知高锰酸钾能氧化草酸.反应如下(部分产物和生成物未写):MnO![]() +H2C2O4→Mn2++CO2↑。若把该反应设计成一原电池,则正极的电极反应式为___。
+H2C2O4→Mn2++CO2↑。若把该反应设计成一原电池,则正极的电极反应式为___。
(2)某同学将2.52g草酸晶体(H2C2O42H2O)加入到100mL0.2molL-1的NaOH溶液中充分反应,测得反应后溶液呈酸性,则其中含碳元素的粒子中物质的量浓度最小的微粒化学式为___。
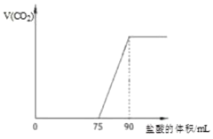
Ⅱ.某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种。
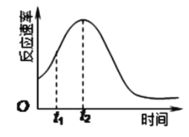
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
(3)猜想Ⅱ可能是:___。
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容。
试管A | 试管B | |
加入试剂 | 2mL0.1mol/LH2C2O4溶液、1mL0.05mol/L酸性KMnO4 | 2mL0.1mol/LH2C2O4溶液、1mL0.05mol/L酸性KMnO4,少量___固体(填物质名称) |
实验现象 (褪色时间) | 褪色时间10min | 褪色时间___10min (选填“<”“>”或“=”) |
结论 | 猜想Ⅱ正确 | |
Ⅲ.为了测定含有H2C2O4·2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0g试样,加水溶解,配成250mL试样溶液。
②用酸式滴定管量取25.00mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500mol/LNaOH溶液滴定,消耗NaOH溶液20.00mL。
③再取25.00mL试样溶液放入另一锥形瓶中,用0.1000mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL。
回答下列问题:
(5)步骤③中判断滴定终点的方法是___。
(6)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得H2C2O4·2H2O的质量分数___。(填“偏大”、“偏小”或“无影响”)