题目内容
【题目】在某温度下,将2molA和3molB充入一密闭容器中,发生反应:aA(g)+B(g) ![]() C(g)+D(g),5min后达到平衡,各物质的平衡浓度的关系为:ca(A)c(B)=c(C)c(D)。若在温度不变的情况下将容器的体积扩大为原来的8倍,A的转化率不发生变化,则B的转化率为( )
C(g)+D(g),5min后达到平衡,各物质的平衡浓度的关系为:ca(A)c(B)=c(C)c(D)。若在温度不变的情况下将容器的体积扩大为原来的8倍,A的转化率不发生变化,则B的转化率为( )
A. 60% B. 40% C. 50% D. 无法确定
【答案】B
【解析】由于平衡浓度关系为ca(A)c(B)=c(C)c(D)mol/L,所以平衡常数K= c(C)c(D)/ ca(A)c(B)=1。在温度不变的情况下将容器的体积扩大为原来的8倍,A的转化率不发生变化,表明减压平衡不移动,a=1。设平衡时消耗xmolA,K= c(C)c(D)/ c(A)c(B)=x2/(2-x)(3-x)=1,x=1.2,则B的转化率为1.2/3=40%,故选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。利用甲醛一定条件下直接脱氢可制甲醛,反应方程式:CH3OH(g)![]() HCHO(g)+H2(g) △H1
HCHO(g)+H2(g) △H1
实验测得随温度升高,平衡常数如下表所示。
温度(K) | 500 | 700 | T1 | T2 | T3 |
平衡常数 | 7.13×10-4 | 3.30×10-1 | 2.00 | 9.00 | 10.00 |
(1)甲醛分子中所有原了都达到稳定结构,甲醛的电子式为_____________。
(2) 若在恒温恒压容器中进行上述反应,可判断反应到达平衡状态的是_______________。
A.混合气体的密度不变
B.CH3OH、HCHO的物质的量浓度之比为1:1
C.H2的体积分数不再改变
D.单位时间内甲醛的生成量与氢气的消耗量相等
(3)T1时,CH3OH、HCHO、H2 起始浓度(mol·L-1)分别为1.0、0.50 、1.0,反应达到平衡时,HCHO 的体积分数___________20% (填“>”、“ =”、“ <”)。
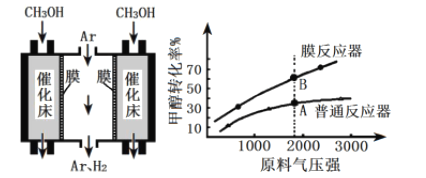
(4)工业上采用膜分离器(对氢气具有很高的选择性和透过率)催化脱氢,装置如下图。为探究转化率变化,分别在普通反应器和膜反应器中,改变原料气压强,控制相同温度,经过相同反应时间,测定甲醇转化率,实验结果如下图。
①A点:v正______v逆(填“>”、“ =”、“ <”),理由是____________;
②B点比A点转化率高的原因是_______________。
(5)体系中加入一定量氧气有利于甲醛的生成。反应体系中存在下列反应:
CH3OH(g)+1/2O2(g)![]() HCHO(g)+H2O(g) △H2
HCHO(g)+H2O(g) △H2
H2(g)+12O2(g)![]() H2O(g) △H3
H2O(g) △H3
则△H2、△H3的大小关系是△H2________△H3(填“>”、“ =”、“ <”)。


