题目内容
10.下列说法正确的是( )| A. | 物质的量是一个基本单位 | |
| B. | 1mol水分子中含有1mol氢分子和1mol氧原子 | |
| C. | 1molH2O的质量等于NA个H2O质量的总和 | |
| D. | 摩尔就是物质的量 |
分析 A.物质的量为国际单位制中7个基本物理量之一;
B.水分子由氢原子与氧原子构成,不含氢气分子;
C.1molH2O含有NA个H2O分子;
D.摩尔是物质的量的单位.
解答 解:A.物质的量为国际单位制中7个基本物理量之一,其单位为摩尔,故A错误;
B.水分子由氢原子与氧原子构成,不含氢气分子,1mol水分子中含有2mol氢原子和1mol氧原子,故B错误;
C.1molH2O含有NA个H2O分子,故1molH2O的质量等于NA个H2O质量的总和,故C正确;
D.摩尔是物质的量的单位,故D错误,
故选C.
点评 本题考查物质的量、摩尔质量,比较基础,注意使用物质的量应指明具体的物质或微粒.

练习册系列答案
相关题目
20.短周期元素W、X、Y和Z的原子序数依次增大.元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍.下列说法错误的是( )
| A. | 元素W、X的氯化物中,各原子均满足8电子的稳定结构 | |
| B. | 元素X与氢可形成原子个数比为1:4的化合物 | |
| C. | 元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 | |
| D. | 元素Z可与元素X形成化合物XZ2 |
1.下列事实不能用元素周期律解释的是( )
| A. | 稳定性:HF>HCl>HBr>HI | |
| B. | 非金属最高氧化物的水化物酸性:HClO4>H2SO4>H2PO4>H2SiO3 | |
| C. | 金属最高价氧化物的水化物碱性:NaOH>Mg(OH)2>Al(OH)3 | |
| D. | 挥发性:HCl>HNO3>H2SO4 |
18.下列说法正确的是( )
| A. | 按系统命名法,化合物 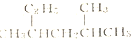 的名称为2-甲基-4-乙基戊烷 的名称为2-甲基-4-乙基戊烷 | |
| B. | 等质量的甲烷、乙烯、乙炔分别充分燃烧,所耗用氧气的量依次减少 | |
| C. | 苯酚、水杨酸(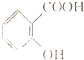 )和苯甲酸都是同系物 )和苯甲酸都是同系物 | |
| D. | 2,2-二甲基-1-丁醇与2-甲基-2-丁醇互为同分异构体 |
5.已知热化学方程式:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98.32kJ•mol-1,在容器中充入2mol SO2和1mol O2,充分反应,最终放出的热量( )
| A. | 等于196.64kJ | B. | 等于98.32kJ | C. | 小于196.64kJ | D. | 大于196.64kJ |
2.某溶液中存在Mg2+、Ag+、Ba2+三种金属离子,现用NaOH、Na2CO3、NaCl三种溶液使它们分别沉淀并分离出,要求每次只加一种溶液,滤出一种沉淀,所加溶液顺序正确的是( )
| A. | Na2CO3 NaCl NaOH | B. | NaOH NaCl Na2CO3 | ||
| C. | NaCl NaOH Na2CO3 | D. | NaCl Na2CO3 NaOH |
19.准确量取25.00mL高锰酸钾溶液,可选用的仪器是( )
| A. | 50 mL量筒 | B. | 10 mL量筒 | C. | 50 mL酸式滴定管 | D. | 50 mL碱式滴定管 |
20.想一想:氢氧化钡(液态)、硫酸铜(固态)、纯碱(固态)这些物质为什么归为一类,下列哪种物质还可以和它们归为一类( )
| A. | C2H5OH(液态) | B. | 盐酸 | C. | 氯化钠溶液 | D. | 豆浆 |