题目内容
【题目】下列说法不正确的是
A. H2O比H2S稳定是因为前者分子间作用力大
B. Na2O和Na2O2中阴、阳离子个数比相同
C. HCl属于共价化合物,溶于水能电离出H+和Cl-
D. 碘单质升华时破坏的是分子间作用力
【答案】A
【解析】
A.稳定性是化学性质,与中心元素的非金属性有关,因为非金属性O>S,所以H2O比H2S稳定,与分子间作用力无关,故A错误;
B. Na2O和Na2O2中阴、阳离子个数比都是1:2,故B正确;
C. HCl属于共价化合物,在水分子的作用下完全电离,为强电解质,故C正确;
D. 碘单质属于分子晶体,升华时破坏的是分子间作用力,故D正确。
故选A。

练习册系列答案
相关题目
【题目】铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的 CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
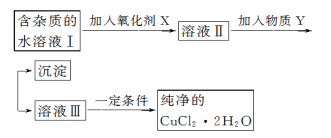
已知Cu2+、 Fe3+和 Fe2+的氢氧化物开始沉淀和沉淀完全时的 pH,见下表:
Fe3+ | Fe2+ | Cu2+ | |
氢氧化物开始沉淀时的 pH | 1.9 | 7.0 | 4.7 |
氢氧化物完全沉淀时的 pH | 3.0 | 9.0 | 6.7 |
请回答下列问题:
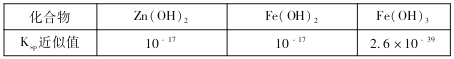
(1)常温下,计算Fe(OH)3的溶度积Ksp=________(通常认为残留在溶液中的离子浓度小于1×10-5 mol/L 时则沉淀完全。)
(2)加入氧化剂的目的______________________。
(3)最适合作氧化剂X的是__________。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(4)加入的物质 Y 是____________。
(5)若向溶液Ⅱ中加入碳酸钙,产生的现象是____________________。