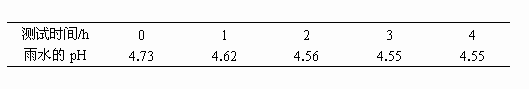题目内容
20世纪60年代,化学家发现了一类酸性比100%的硫酸还要强的酸,称之为魔酸,其酸性强至可以将质子给予δ受体,CF3SO3H就是其中常见的魔酸之一。
⑴ 试写出CH3CH3与CF3SO3H可能的反应式。
⑵ 以上反应所得产物活性均很高,立即发生分解,试写出分解以后所得到的全部可能产物。
⑴  (2.5分)
(2.5分)
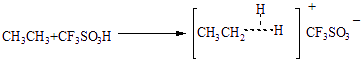 (2.5分)
(2.5分)
(生成二电子三中心键)
⑵ 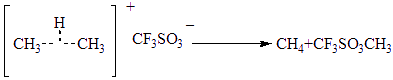
(1分) (1分)
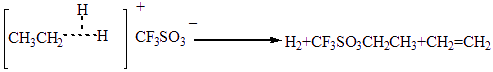
(1分) (1分) (1分)
解析:
⑴根据题意,CF3SO3H是魔酸,能够将质子给予σ键,在CH3CH3中,存在两种类型的σ键:C-C键和C-H键,因此可能生成两种类型的二电子三中心键,即:

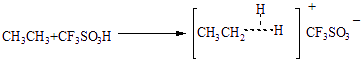
⑵以上生成的两种物质均属于缺电子的物质,因此发生分解反应,中间产物为存在碳正离子,如CH3+,CH3CH2+,它们都能与CF3SO3-结合生成取代磺酸。CH3CH2+还能发生消去反应,生成烯烃——CH2=CH2 。

 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下:
测试时间/h | 0 | 1 | 2 | 3 | 4 |
雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
分析数据,回答下列问题:
①雨水样品的pH变化的原因是(用化学方程式表示)________________。
②如果将刚取样的上述雨水和自来水相混合,pH将变________,原因是(用化学方程式表示)________。
(2)你认为减少酸雨产生的途径可采用的措施是________。
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
(3)有人在英国进行的一项研究结果表明:高烟囱可以有效地降低地表面SO2浓度。在20世纪60~70年代的10年间,由发电厂排放出的SO2增加了35%,但由于建造高烟囱,使地面浓度降低了30%之多。请你从全球环境保护的角度,分析这种方法是否可取?简述其理由。______________________________________________
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下:
测定时间/h | 0 | 1 | 2 | 3 | 4 |
雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
分析数据,回答下列问题:
①雨水样品的pH变化的原因是(用化学方程式表示)_______________________。
②如果将刚取样的上述雨水和自来水混合,pH将变,原因是(用化学方程式表示)____
_______________________。
(2)你认为减少酸雨产生的途径可采取的措施是__________。
①少用煤作燃料 ②把工厂烟囱造高 ③燃烧脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
(3)英国的一项研究结果表明:高烟囱可以有效地降低地表面SO2的浓度。在20世纪60—70年代间,由发电厂排出的SO2增加了35%,但由于建筑高烟囱的结果,地面浓度降低了30%之多。请你从全球环境保护的角度,分析这种方法是否可取?简述其理由。