题目内容
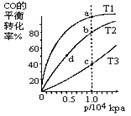
下列表格中的各种情况,可以用下面的图象曲线表示的是
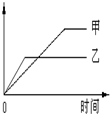

| | 反应 | 纵坐标 | 甲 | 乙 |
| A | 等质量钾、钠分别与足量水反应 | H 2质量 | 钠 | 钾 |
| B | 相同质量氨气,在同一容器中 2NH3 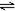 N2+3H2 ΔH >0 N2+3H2 ΔH >0 | 氨气的转化率 | 500℃ | 400℃ |
| C | 在体积可变的恒压容器中,体积比1:3的N2、H2,N2+3H2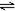 2NH3 2NH3 | 氨气的浓度 | 活性一般的催化剂 | 活性高的催化剂 |
| D | 2molSO2与lmolO2,在相同温度下2SO2(g)+O2(g)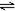 2SO3(g) 2SO3(g) | SO3物质的量 | 2个大气压 | 10个大气压 |
A
试题分析:A.K、Na都是+1价的金属,都能与水反应置换出H2,由于M(K)>M(Na),所以等质量时放出的氢气Na比K多,而金属活动性K>Na,所以反应时K比Na快。因此该选项正确。B.对于任何化学反应,升高温度,化学反应速率加快,达到平衡所需要的时间缩短。因此500℃要先达到平衡。即显出现拐点。错误。C. 对于一个确定的化学反应,当起始时投入的物质的配比相同时,如果其它条件都相同,只有催化剂不同,则由于催化剂只是改变反应途径,不能使化学平衡发生移动,所以平衡时氨气的浓度不变。错误。D.反应2SO2(g)+O2(g)
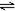 2SO3(g)是个气体体积减小的反应。增大压强,气体的浓度增大,反应速率加快,达到平衡所需要的时间缩短。即显出现拐点。增大压强,根据平衡移动原理,化学平衡正向移动,产生更多的SO3。所以平衡时SO3物质的量增多。错误。2的多少的知识。
2SO3(g)是个气体体积减小的反应。增大压强,气体的浓度增大,反应速率加快,达到平衡所需要的时间缩短。即显出现拐点。增大压强,根据平衡移动原理,化学平衡正向移动,产生更多的SO3。所以平衡时SO3物质的量增多。错误。2的多少的知识。
练习册系列答案
相关题目
 pC(g)+qD(g)平衡常数为K,下列说法正确的是( )
pC(g)+qD(g)平衡常数为K,下列说法正确的是( ) C(g)+D(g)已达到平衡状态( )
C(g)+D(g)已达到平衡状态( )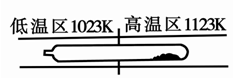
 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下: CO2(g) + H2 (g)在一定条件下的密闭容器中,该反应达到化学平衡状态。请回答:
CO2(g) + H2 (g)在一定条件下的密闭容器中,该反应达到化学平衡状态。请回答: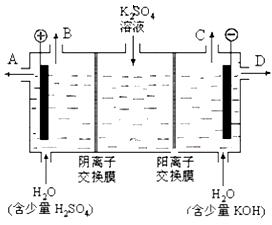
 CH3OH(g) △H<0
CH3OH(g) △H<0