题目内容
Cl2和水所发生的反应:Cl2+H2O![]() HClO+HCl,在化学反应中称之为歧化反应。试分析下列反应中,不属于歧化反应的是()
HClO+HCl,在化学反应中称之为歧化反应。试分析下列反应中,不属于歧化反应的是()
A.3NO![]() +H
+H![]() O
O![]() 2HNO
2HNO![]() +NO
+NO
B.2Na![]() O
O![]() +2CO
+2CO![]()
![]() 2Na
2Na![]() CO
CO![]() +O
+O![]()
C.NO+NO![]() +2NaOH
+2NaOH![]() 2NaNO
2NaNO![]() +H
+H![]() O
O
D.P4+3KOH+3H2O![]() 3KH2PO2+PH3
3KH2PO2+PH3
C
解析:
歧化反应的特点是:同一种元素中间价态低价态+高价态,而C选项是高价态+低价态中间价态,属于归中反应,故选C。

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
 某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现在足量的稀氯化亚铁溶液中加入1~2滴溴水,振荡后溶液呈黄色.
某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现在足量的稀氯化亚铁溶液中加入1~2滴溴水,振荡后溶液呈黄色.(1)提出问题:Fe3+、Br2的氧化性哪个更强?
(2)猜想:①甲同学认为氧化性:Fe3+>Br2,故上述实验现象是因为溶液中含
②乙同学认为氧化性:Fe3+<Br2,故上述实验现象是发生化学反应所致,则溶液呈黄色是含
(3)设计实验并验证,丙同学为验证乙同学的观点,选用下列某些试剂,设计了两种方案进行实验.通过观察实验现象,证明乙同学的观点是正确的.
供选用的试剂:a.酚酞试液 b.四氯化碳 c.无水酒精 d.硫氰化钾溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象(试剂填序号)
| 编号 | 选用试剂 | 实验现象 |
| 方案1 | ||
| 方案2 |
氧化性:Fe3+<Br2.写出在足量的稀氯化亚铁溶液中加入1~2滴溴水的离子反应方程式
(5)结论应用
在2mol FeBr2溶液中通入一定量的Cl2,当有33.6L Cl2(标准状况)与FeBr2溶液发生反应时,所发生的离子反应方程式为
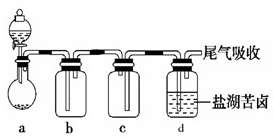
(6)某同学用图所示的实验装置制取氧化剂Cl2并将其通入盐湖苦卤中.装置c在实验中的作用是
A.制NH3:浓氨水和碱石灰
B.制SO2:Cu片和浓硫酸
C.制NO:Cu片和稀硝酸
D.制O2:MnO2和双氧水.
