题目内容
铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是 ;Y与过量浓硝酸反应后溶液中含有的盐的化学式为 。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是 。
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
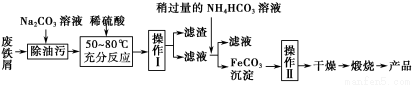
回答下列问题:
①操作Ⅰ的名称是 ;操作Ⅱ的名称是 ;操作Ⅱ的方法为 。
②请写出生成FeCO3沉淀的离子方程式: 。
(1)Fe2+、Fe3+、H+ Fe(NO3)3
(2)BC
(3)①过滤 洗涤 在漏斗中加入适量蒸馏水,浸没沉淀,让蒸馏水自然流下,重复2~3次 ②Fe2++2HCO3-=FeCO3↓+CO2↑+H2O
【解析】(1)铁的氧化物中具有磁性的是Fe3O4,Fe3O4溶于过量的盐酸后溶液中存在的阳离子是Fe2+、Fe3+、H+;Fe3O4溶于过量的浓硝酸后Fe元素会被氧化为Fe3+,所以反应后的溶液中含有的盐是Fe(NO3)3。(2)向该溶液中加入过量的NaOH溶液后:Mg2+→Mg(OH)2、Fe2+→Fe(OH)3、Al3+→AlO2-、Cu2+→Cu(OH)2;过滤后滤渣中含有Mg(OH)2、Fe(OH)3、Cu(OH)2;高温灼烧后Mg(OH)2→MgO、Fe(OH)3→Fe2O3、Cu(OH)2→CuO;将MgO、Fe2O3、CuO投入过量盐酸后生成Mg2+、Fe3+、Cu2+,故应选择B、C。(3)①从流程图中知道经操作Ⅰ得到滤渣,故该操作是过滤;操作Ⅱ是在得到FeCO3沉淀后进行的,故该操作是洗涤;洗涤具体操作方法为:在漏斗中加入适量蒸馏水,浸没沉淀,让蒸馏水自然流下,重复2~3次;②从流程图中分析加入稍过量的NH4HCO3溶液,有FeCO3沉淀,还应有CO2生成,发生复分解反应的离子方程式为:Fe2++2HCO3-=FeCO3↓+CO2↑+H2O。

 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案