题目内容
下列叙述中,正确的是
- A.在标准状况下,1mol任何物质的体积为22.4L
- B.等物质的量浓度的盐酸和硫酸中,H+的物质的量浓度也相等
- C.1molH2和1molHe中,所含的分子数相同、原子数相同、质量也相同
- D.体积为6L的O2,其质量可能为8g
D
分析:A.根据气体摩尔体积是使用范围分析;
B.强酸溶液中氢离子浓度与酸的浓度、酸的元数有关;
C.根据N(分子数)=nNA、m=nM及分子的构成计算判断;
D.根据m=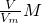 计算其质量.
计算其质量.
解答:A.气体摩尔体积只适用于气体,对固体和液体不适用,所以标况下,1mol任何物质的体积不一定为22.4L,故A错误;
B.强酸溶液中氢离子浓度与酸的浓度、酸的元数有关,盐酸是一元酸,硫酸是二元酸,等物质的量浓度的盐酸和硫酸中,硫酸中氢离子物质的量浓度是盐酸中氢离子物质的量浓度的2倍,故B错误;
C.根据N(分子数)=nNA、m=nM及分子的构成知,1molH2和1molHe中,所含的分子数相同,原子数和质量不同,故C错误;
D.温度和压强未知,所以气体摩尔体积未知,根据m=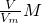 知,6L的O2,其质量可能为8g,故D正确;
知,6L的O2,其质量可能为8g,故D正确;
故选D.
点评:本题考查了气体摩尔体积的使用范围、物质的量的有关计算等知识点,注意氦气是单原子分子不是双原子分子,为易错点.
分析:A.根据气体摩尔体积是使用范围分析;
B.强酸溶液中氢离子浓度与酸的浓度、酸的元数有关;
C.根据N(分子数)=nNA、m=nM及分子的构成计算判断;
D.根据m=
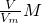 计算其质量.
计算其质量.解答:A.气体摩尔体积只适用于气体,对固体和液体不适用,所以标况下,1mol任何物质的体积不一定为22.4L,故A错误;
B.强酸溶液中氢离子浓度与酸的浓度、酸的元数有关,盐酸是一元酸,硫酸是二元酸,等物质的量浓度的盐酸和硫酸中,硫酸中氢离子物质的量浓度是盐酸中氢离子物质的量浓度的2倍,故B错误;
C.根据N(分子数)=nNA、m=nM及分子的构成知,1molH2和1molHe中,所含的分子数相同,原子数和质量不同,故C错误;
D.温度和压强未知,所以气体摩尔体积未知,根据m=
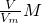 知,6L的O2,其质量可能为8g,故D正确;
知,6L的O2,其质量可能为8g,故D正确;故选D.
点评:本题考查了气体摩尔体积的使用范围、物质的量的有关计算等知识点,注意氦气是单原子分子不是双原子分子,为易错点.

练习册系列答案
相关题目
下列叙述中不正确的是( )
| A、第ⅠA族的金属元素是同一周期中金属性最强的元素 | B、P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强 | C、元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 | D、主族元素原子的最外层电子数不一定等于该元素的最高化合价 |
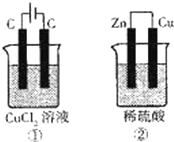 如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol?L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述中不正确的是( )
如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol?L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述中不正确的是( )