��Ŀ����
7����һ��������ܱ������У��������»�ѧ��Ӧ��CO2��g��+H2��g���TCO��g��+H2O��g�����仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���| T/�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
��1���÷�ӦΪ���ȷ�Ӧ������ȡ��������ȡ�����
��2����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����bc��
a����ʱ�����CO���� b���ʵ������¶�
c������CO2��Ũ�� d��ѡ���Ч����
��3�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������bc����ѡ���÷֣���
a��������ѹǿ���� b����������� c��CO������
c��v����H2��=v����H2O�� d��c��CO2��=c��CO��
��4��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c��CO2��•c��H2��=c��CO��•c��H2O�������жϴ�ʱ���¶�Ϊ830�森
��5�����ڣ�4���������¶��£���1L���ܱ������У�����2molCO2��3molH2��ַ�Ӧ��ƽ��ʱ��H2�����ʵ���Ϊb��CO2�����ʵ���Ϊc��
a������1.0mol b������1.0mol c������0.5mol��С��1.0mol d����ȷ����
���� ��1�������¶ȶԻ�ѧƽ�⡢��ѧƽ�ⳣ����Ӱ�����ش�ƽ�ⳣ�����¶���������˵��ƽ��������У�
��2�����¡���ѹ������Ũ�ȡ�ʹ�ô�������ʹ�÷�Ӧ�ķ�Ӧ���������ݻ�ѧƽ���ƶ�ԭ��ȷ��ƽ����ƶ�����
��3����ѧƽ��״̬�ı�־�����淴Ӧ������ȣ�����ֺ������ֲ��䣬�ݴ˻ش�
��4��ij�¶��£������ʵ�ƽ��Ũ�ȷ�����ʽ��c��CO2����c��H2��=c��CO����c��H2O����˵�� K=1���ɴ˷������
��5�����ݻ�ѧƽ������ʽ��ʽ��ƽ�ⳣ��������������������ʵ�������õ�ƽ��״̬�µ����ʵ�����
��� �⣺��1����ѧƽ�ⳣ���Ĵ�Сֻ���¶��йأ������¶ȣ�ƽ�������ȵķ����ƶ����ɱ���֪�������¶ȣ���ѧƽ�ⳣ������˵����ѧƽ�������ƶ����������Ӧ�������ȣ�
�ʴ�Ϊ�����ȣ�
��2��a����ʱ�����CO���壬��ʹ�÷�Ӧ�ķ�Ӧ���ʽ��ͣ��ʴ���
b���ʵ������¶ȣ���ʹ�÷�Ӧ�ķ�Ӧ��������ƽ��������Ӧ�����ƶ�������ȷ��
c������CO2��Ũ�ȣ���ʹ�÷�Ӧ�ķ�Ӧ��������ƽ��������Ӧ�����ƶ�������ȷ��
d��ѡ���Ч��������ʹ�÷�Ӧ�ķ�Ӧ���������Dz�����ƽ����ƶ����ʴ���
��ѡbc��
��3��a����Ӧ��һ����Ӧǰ���������ķ�Ӧ��ѹǿ�ĸı䲻��Ҫ����ƽ���ƶ����ʴ���
b����ѧƽ��ʱ������ֵ�Ũ�Ȳ���ʱ��ĸı���ı䣬����ȷ��
c����ѧƽ��״̬�ı�־��v��=v��������v����H2��=v����H2O��������Ӧ�ﵽƽ��״̬����C��ȷ��
d��c��CO2��=c��CO��ʱ�����ܱ������淴Ӧ������ȣ���һ���ﵽ��ƽ��״̬���ʴ���
��ѡbc��
��4��ij�¶��£������ʵ�ƽ��Ũ�ȷ�����ʽ��c��CO2����c��H2��=c��CO����c��H2O����˵�� K=1����Ӧ���¶���830�棬�ʴ�Ϊ��830��
��5�����ڣ�3���������¶��£���1L���ܱ������У�����2mol CO2��3mol H2��ַ�Ӧ��ƽ��ʱ���������������ʵ���Ϊx��
CO2��g��+H2��g��?CO��g��+H2O��g��
��ʼ����mol/L�� 2 3 0 0
�仯����mol/L�� x x x x
ƽ������mol/L�� 2-x 3-x x x
K=$\frac{{x}^{2}}{��2-x��•��3-x��}$=1������õ���x=1.2����Ӧ��ƽ��ʱ��H2�����ʵ���3mol-1.2mol=1.8mol��CO2�����ʵ���Ϊ0.8mol��
�ʴ�Ϊ��b��c��
���� ���⿼��ѧ����ƽ�ⳣ��K�ĸı���ƽ���ƶ�֮��Ĺ�ϵ�����⣬�Լ�Ӱ�컯ѧƽ������أ�������ƽ�ⳣ��K���мļ����������ѶȲ���

| A�� | �����¶� | B�� | ����ѹǿ����N2 | ||
| C�� | ����������䣬����O2 | D�� | ����ѹǿ |
| A�� | Na��ˮ��Ӧ��Na+H2O�TNa++OH-+H2�� | |
| B�� | ���ˮ�еμӱ���FeCl3��Һ�Ʊ�Fe��OH��3���壺Fe3++3H2O$\frac{\underline{\;V\;}}{\;}$Fe��OH��3��+3H+ | |
| C�� | ʵ����ʢװNaOH��Һ���Լ�ƿ�����ò�������SiO2+2OH-�TSiO32-+H2O | |
| D�� | ��̼�������Һ�м������������������Һ��Ca2++OH-+HCO3-�TCaCO3��+H2O+CO32- |
| A�� |  | B�� | 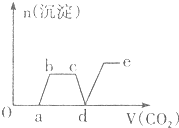 | ||
| C�� | 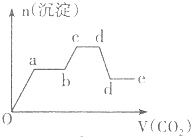 | D�� |  |
| A�� | ��H2SO4��Һ�м���Ba��OH��2��Һ | B�� | ��AlCl3��Һ��ͨ�백�� | ||
| C�� | ��Na2S��Һ��ͨ��SO2 | D�� | ��Fe2��SO4��3��Һ�м���Cu |
| CaCO3 | CaSO4 | Mg��OH��2 | MgCO3 |
| 1.4��10-3 | 2.55��10-2 | 9��10-4 | 1.1��10-2 |
| A�� | ���������Һ�д���CaSO4��s��?Ca2+��aq��+SO42-��aq�� | |
| B�� | ��Na2CO3��Һ���ݹ�¯�е�ˮ�����ɽ�ˮ���е�CaSO4ת��ΪCaCO3 | |
| C�� | ��Mg��OH��2����Һ�еμ�FeCl3��������Ϊ���ɫ��˵���ܽ��Fe��OH��3��Mg��OH��2 | |
| D�� | ��2ml����MgCl2 ��Һ���Ⱥ�μ�0.1mol/L��Na2CO3��NaOH��Һ��2�Σ������İ�ɫ����ΪMg��OH��2 |
 ѧУ��ѧ�о�С���ij��Һ���м�����������ɫ��Һ�п��ܺ���NH4+��K+��Al3+��HCO3-��Cl-��MnO4-��SO42-�������еļ������ӣ�
ѧУ��ѧ�о�С���ij��Һ���м�����������ɫ��Һ�п��ܺ���NH4+��K+��Al3+��HCO3-��Cl-��MnO4-��SO42-�������еļ������ӣ�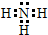 ���ռ乹��Ϊ�����Σ�
���ռ乹��Ϊ�����Σ�