题目内容
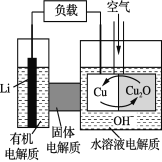
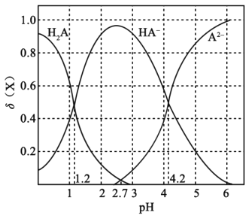
【题目】改变0.1mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数φ(X)随pH的变化如图所示。
下列叙述错误的是( )
A.pH=1.2时,c(H2A)=c(HA-)
B.lg[K2(H2A)]=-4.2
C.pH=2.7时,c(HA-)>c(H2A)=c(A2-)
D.pH=4.2时,c(HA-)=c(A2-)=c(H+)
【答案】D
【解析】
由图象可知,pH=1.2时,c(H2A)=c(HA-),pH=2.7时,c(H2A)=c(A2-),pH=4.2时,c(HA-)=c(A2-),随着pH的增大,c(H2A)逐渐减小,c(HA-)先增大后减小,c(A2-)逐渐增大,结合电离平衡常数以及题给数据计算,可根据纵坐标比较浓度大小,以此解答该题。
A.由图象可知pH=1.2时,H2A与HA-的曲线相交,则c(H2A)=c(HA-),A正确;
B.pH=4.2时,c(H+)=10-4.2mol/L,c(HA-)=c(A2-),K2 (H2A)=![]() =10-4.2,则lg[K2(H2A)]=-4.2, B正确;
=10-4.2,则lg[K2(H2A)]=-4.2, B正确;
C.由图象可知,pH=2.7时,c(H2A)=c(A2-),由纵坐标数据可知c(HA-)>c (H2A)=c(A2-),C正确;
D.pH=4.2时,c(HA-)=c(A2-),但此时c (H2A)≈0,如体积不变,则c(HA-)=c(A2-)=0.05molL-1,c(H+)=10-4.2mol/L,如体积变化,则不能确定c(HA-)、c(A2-)与c(H+)浓度大小关系,D错误。
答案为D。

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目