题目内容
(10分) I.已知下列三个热化学方程式
①H2(g)+O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
③C(s)+H2O(g)===CO(g)+H2(g) ΔH=+131 kJ·mol-1
写出表示碳不完全燃烧生成CO的热化学方程式。__________;
II. 氨气溶于水得到氨水,在25℃下,将a mol·L-1的氨水与b mol·L-1的盐酸等体积混合,反应后溶液显中性,则用含a和b的代数式表示出该混合溶液中氨水的电离平衡常数 。
III.下列5种有机化合物:水杨酸( )、苯酚( )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
①其中能与Na2CO3溶液反应,但不能与FeCl3溶液发生显色反应的是 。(填化学式)
②其中能与FeCl3溶液发生显色反应,但不能与NaHCO3溶液反应的是 。(填化学式)
③写出水杨酸与金属钠反应的化学方程式 。
①H2(g)+O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
③C(s)+H2O(g)===CO(g)+H2(g) ΔH=+131 kJ·mol-1
写出表示碳不完全燃烧生成CO的热化学方程式。__________;
II. 氨气溶于水得到氨水,在25℃下,将a mol·L-1的氨水与b mol·L-1的盐酸等体积混合,反应后溶液显中性,则用含a和b的代数式表示出该混合溶液中氨水的电离平衡常数 。
III.下列5种有机化合物:水杨酸( )、苯酚( )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
①其中能与Na2CO3溶液反应,但不能与FeCl3溶液发生显色反应的是 。(填化学式)
②其中能与FeCl3溶液发生显色反应,但不能与NaHCO3溶液反应的是 。(填化学式)
③写出水杨酸与金属钠反应的化学方程式 。
C(s)+O2(g)===CO(g) ΔH=-110.8 kJ·mol-1(2分)
II.K= (2分)III.①乙酸(CH3COOH )②苯酚(
(2分)III.①乙酸(CH3COOH )②苯酚(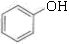 )
)
II.K=
 (2分)III.①乙酸(CH3COOH )②苯酚(
(2分)III.①乙酸(CH3COOH )②苯酚( )
)I.根据盖斯定律可知,①+③即得到C(s)+O2(g)==="CO(g)" ,所以反应热是△H=-241.8 kJ·mol-1+131 kJ·mol-1=-110.8 kJ·mol-1。
II.反应后显中性,说明氨水过量。剩余氨水的浓度是 ,根据电荷守恒可知,溶液中NH4+浓度是
,根据电荷守恒可知,溶液中NH4+浓度是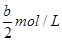 、OH-浓度是10-7mol/L,所以氨水的电离平衡常数为.K=
、OH-浓度是10-7mol/L,所以氨水的电离平衡常数为.K= =
= 。
。
III.考查常见官能团的性质。
①能与Na2CO3溶液反应,但不能与FeCl3溶液发生显色反应,说明含有羧基,但不能含有酚羟基,所以应该是乙酸。
②能与FeCl3溶液发生显色反应,但不能与NaHCO3溶液反应,说明含有酚羟基,但没有羧基,所以应该是苯酚。
II.反应后显中性,说明氨水过量。剩余氨水的浓度是
 ,根据电荷守恒可知,溶液中NH4+浓度是
,根据电荷守恒可知,溶液中NH4+浓度是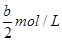 、OH-浓度是10-7mol/L,所以氨水的电离平衡常数为.K=
、OH-浓度是10-7mol/L,所以氨水的电离平衡常数为.K= =
= 。
。III.考查常见官能团的性质。
①能与Na2CO3溶液反应,但不能与FeCl3溶液发生显色反应,说明含有羧基,但不能含有酚羟基,所以应该是乙酸。
②能与FeCl3溶液发生显色反应,但不能与NaHCO3溶液反应,说明含有酚羟基,但没有羧基,所以应该是苯酚。

练习册系列答案
相关题目
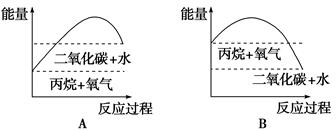
 2SO3(g) △H=-196.64kJ/mol,当放出314.624kJ热量时,SO2的转化率为( )
2SO3(g) △H=-196.64kJ/mol,当放出314.624kJ热量时,SO2的转化率为( )
 2Fe(s)+3CO2(g) ΔH="-a" kJ/mol
2Fe(s)+3CO2(g) ΔH="-a" kJ/mol