题目内容
【题目】某有机物的结构简式如图所示,有关该有机物的叙述不正确的是
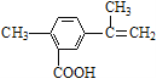
A. 在一定条件下,能发生取代、酯化和加聚反应
B. 该物质能使酸性KMnO4溶液褪色
C. lmol该物质最多可与5molH2发生加成反应
D. lmol该物质完全燃烧最多可消耗13mol氧气
【答案】C
【解析】
A.结构中含-COOH,能发生取代反应、酯化反应,含碳碳双键可发生加聚反应,故A正确;
B.结构中含碳碳双键、苯环上含有侧链烃基,都能使酸性KMnO4溶液褪色,故B正确;
C.苯环、碳碳双键能够与氢气发生加成反应,则1mol物质最多可与4molH2发生加成反应,故C错误;
D.分子中含11个C、12个H、2个O,则1mol该物质完全燃烧最多可消耗氧气为1mol×(11+![]() -
-![]() )=13mol,故D正确;
)=13mol,故D正确;
答案选C。

练习册系列答案
相关题目
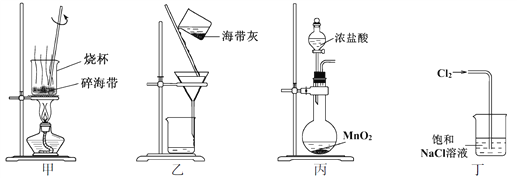
【题目】下列各项操作或现象能达到预期实验目的的是
选项 | 操作或现象 | 实验目的 |
A | 将铁钉放入试管中,用盐酸浸没 | 验证铁的吸氧腐蚀 |
B | 向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色 | 证明Br—还原性强于Cl— |
C | 将氯化亚铁固体溶于适量蒸馏水中 | 配制FeCl2溶液 |
D | 将混有氯化氢杂质的氯气通过装有饱和NaHCO3溶液的洗气瓶 | 除去氯气中的HCl气体 |
A. A B. B C. C D. D