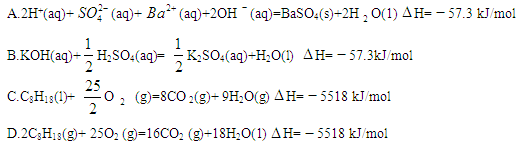题目内容
有关化学反应热效应及反应自发性的下述描述,其中正确的是
| A.由CH3(CH2)2CH3(g)+13/2O2(g)=4CO2(g)+5H2O(g) △H= -2658 kJ·mol-1,可知正丁烷的燃烧热为:-2658 kJ·mol-1。 |
| B.OH(aq)-+ H(aq)+ = H2O(l)△H=-57.3kJ?mol-1, 故1mol醋酸与1molNaOH完全反应,放出的热量一定为57.3kJ |
| C.2CO(g)+O2(g)===2CO2(g); ΔH=-566 kJ·mol-1,N2(g)+O2(g)===2NO(g);ΔH=+180 kJ·mol-1,则2CO(g)+2NO(g)===N2(g)+2CO2(g)的ΔH=-746 kJ·mol-1 |
D.若反应2AB(g) C(g) + 3D(g) 在高温下能自发进行,其逆反应在低温下能自发进行,则该正反应的△H<0、△S>0 C(g) + 3D(g) 在高温下能自发进行,其逆反应在低温下能自发进行,则该正反应的△H<0、△S>0 |
C
A、燃烧热中水为液体;
B、醋酸的电离吸热,故小于57.3KJ;
C、运用盖斯定律,正确;
D、正反应为吸热
B、醋酸的电离吸热,故小于57.3KJ;
C、运用盖斯定律,正确;
D、正反应为吸热

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目