题目内容
对于达到平衡状态的可逆反应N2(g)+3H2(g)?2NH3(g)正反应为放热反应下列叙述中正确的是( )
| A、c(N2):c(H2):c(NH3)=1:3:2 | B、N2、H2 和NH3 浓度不再变化说明已达平衡 | C、增大压强不利于氨的合成 | D、N2与H2的物质的量之和是氨气的物质的量的2倍 |
分析:化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度、质量、物质的量以及百分含量等不变,由此衍生的一些物理量不变;根据压强增大,平衡向气体体积减少的方向移动.
解答:解:A.达到平衡状态时,反应物和生成物的浓度不再发生变化,但各物质的浓度之比不一定等于系数之比,故A错误;
B.达到平衡状态时,反应物和生成物的浓度不再发生变化,故B正确;
C.增大压强,平衡向正反应移动,有利于氨的合成,故C错误;
D.达到平衡状态时,反应物和生成物的物质的量不再发生变化,但N2与H2的物质的量之和不一定是氨气的物质的量的2倍,故D错误;
故选:B.
B.达到平衡状态时,反应物和生成物的浓度不再发生变化,故B正确;
C.增大压强,平衡向正反应移动,有利于氨的合成,故C错误;
D.达到平衡状态时,反应物和生成物的物质的量不再发生变化,但N2与H2的物质的量之和不一定是氨气的物质的量的2倍,故D错误;
故选:B.
点评:本题考查平衡状态的判断以及外界条件对化学平衡的影响,题目难度中等,注意注意反应前后的气体的化学计量数关系.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
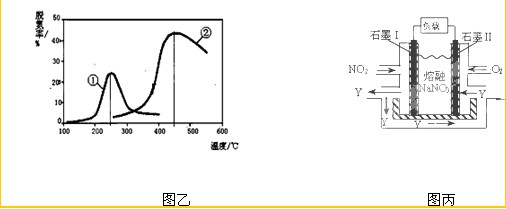
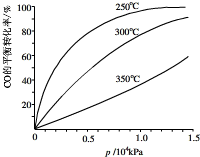 (2013?闵行区二模)研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(2013?闵行区二模)研究NO2、SO2、CO等大气污染气体的处理具有重要意义.