题目内容
10.下列实验问题的处理方法中,正确的是( )| A. | 蔗糖溶液加入稀硫酸共热后,加入银氨溶液,水浴加热,检验水解产物具有还原性 | |
| B. | 在气体发生装置上直接点燃甲烷时,必须先检验甲烷的纯度 | |
| C. | 不慎将苯酚溶液沾到皮肤上,要立即用强碱溶液冲洗 | |
| D. | 为提纯蛋白质,可向鸡蛋清溶液中加入醋酸铅溶液,然后将所得沉淀滤出重新溶于水,即得较纯的蛋白质溶液 |
分析 A.银镜反应必须在碱性条件下;
B.甲烷点燃时易产生爆炸,所以点燃前必须验纯;
C.强碱溶液具有强腐蚀性;
D.重金属盐能使蛋白质发生变性,铵盐溶液可以使蛋白质发生盐析.
解答 解:A.银镜反应必须在碱性条件下,所以蔗糖溶液发生水解后应该先加NaOH中和剩余的酸,然后滴加银氨溶液,故A错误;
B.甲烷点燃时易产生爆炸,所以点燃前必须验纯,否则易产生安全事故,故B正确;
C.强碱溶液具有强腐蚀性,苯酚易溶于酒精溶液,所以不慎将苯酚溶液沾到皮肤上,应立即用酒精洗涤,再用水冲洗,故C错误;
D.重金属盐能使蛋白质发生变性,铵盐溶液可以使蛋白质发生盐析,醋酸铅是重金属盐,能使蛋白质发生变性,应该用硫酸铵溶液分离提纯蛋白质,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及蛋白质变性和盐析、实验安全、银镜反应等知识点,明确实验原理及物质性质是解本题关键,易错选项是D,注意蛋白质发生盐析和变性的区别,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11. 某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:
某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:
①第一份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为9.32g.
②第二份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.
已知:2Al3++2CO32-+3H2O=2Al(OH)3↓+3CO2↑
(1)由此推断,原溶液一定含有的阳离子种类及其浓度,将结果填入下表(可不填满).
(2)无法确定的离子是NO3-,如何通过进一步实验确证未确定的离子是否存在?用小试管取少量溶液,加入少量浓硫酸,再向试管中加入铜屑并加热,产生的气体在空气中变成红棕色证明含有硝酸根离子..
 某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:
某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:①第一份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为9.32g.
②第二份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.
已知:2Al3++2CO32-+3H2O=2Al(OH)3↓+3CO2↑
(1)由此推断,原溶液一定含有的阳离子种类及其浓度,将结果填入下表(可不填满).
| 一定含有的阳离子种类 | ||||||
| 物质的量浓度(mol/L) |
1.在前一种分散系中慢慢地滴入后一种溶液所观察到的现象不是先沉淀后变澄清的是( )
| A. | 氢氧化铁胶体滴加盐酸 | B. | 四羟基合铝酸钠溶液中加盐酸 | ||
| C. | 氯化铝溶液中滴加氢氧化钠溶液 | D. | 氯化铝溶液中滴加氨水 |
2.25℃时,[NH4+]浓度均为1mol/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2三种溶液,若其浓度分别为a、b、c(单位:mol/L),则下列判断正确的是( )
| A. | a=b=c | B. | c>a>b | C. | b>a>c | D. | a>c>b |
19.在无色透明的未知溶液中加入BaCl2溶液生成不溶于稀硝酸的白色沉淀,则未知溶液中可能大量存在( )
| A. | Ag+ | B. | SO42- | C. | CO32- | D. | OH- |
20.下列物质中,最不容易被酸雨腐蚀的是( )
| A. | 铜制塑像 | B. | 大理石雕刻 | C. | 水泥制品 | D. | 铝合金门窗 |

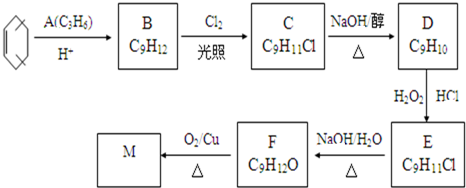
 ;
; ;
;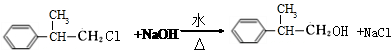 .
.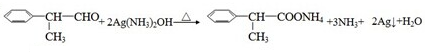 .
.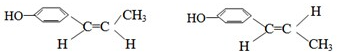 .
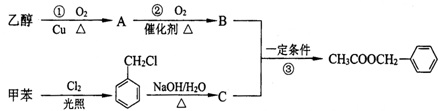
.
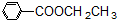 、
、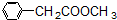 、
、
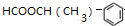 和
和 .
.