题目内容
五种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
请回答下列问题:
(1)元素X位于周期表中第 周期, 族;
(2)这些元素的氢化物中,稳定性最强的是 (写化学式);
(3)Y与N形成的化合物中,Y可能的化合价有 ;
(4)M、Z的原子半径
(填“>”、“<”或“=”)。
(1)二(1分),ⅥA族(1分)
(2)(1分)
(3)+1+2+3+4+5(2分)
(4)>(1分)
解析:略

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
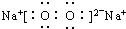
 ]2-Na+
]2-Na+ B的最外层电子数比K层电子多1,D元素的主族序数是周期序数的2倍,E的单质是黄绿色气体;据此填空:
B的最外层电子数比K层电子多1,D元素的主族序数是周期序数的2倍,E的单质是黄绿色气体;据此填空: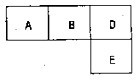 有M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答:
有M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答: