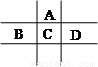题目内容
(17分)有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
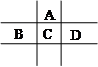
⑴五种元素的名称:A__________,B______________,C____________,D_____________,E______________。
(2)E的最高价氧化物的水化物和NaOH反应的离子方程式是__________________________________________________
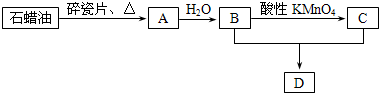
(3) 将C的不稳定氧化物和D的单质等物质的量同时通入到品红溶液中,观察到的现象是___________________________,有关反应的离子方程式为________________。
(4)请设计一个简单实验比较A、C的非金属性的强弱:
(17分)
(1)A:氧 B:磷 C:硫 D:氯 E:铝 (各1分,共5分)
(2)Al(OH)3+ OH -=== [Al(OH)4]- (3分)
(3) 品红不褪色(3分)
SO2 + Cl2 +2H2O = 4H+ + SO42- + 2Cl-(3分)
(4) 将氧气通入到氢硫酸溶液中,溶液出现浑浊。(3分)
解析:

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目