题目内容
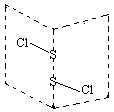
硫的卤化物(S2X2)是广泛用于橡胶工业的硫化剂,S2C12分子结构如图所示。遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2C12+2H2O=SO2↑+3S↓+4HCl。下列说法中错误的是( )

| A.稳定性S2C12>S2Br2 |
| B.反应中,生成1molSO2,转移电子为3mol |
| C.分子中同时含有极性键和非极性键且各原子都满足8电子稳定结构 |
| D.因为S-Cl键能比S-Br键能大,S2C12沸点比S2Br2高 |
D
试题分析:A. S2C12和S2Br2结构相似。元素的非金属性越强,其对应的化合物就越稳定。所以稳定性S2C12>S2Br2。正确。B. 在2S2C12+2H2O=SO2↑+3S↓+4HCl反应中,S的化合价由反应前S2C12的+1变为反应后SO2中的+4价和S的0价。所以生成1molSO2,转移电子为3mol。正确。C.在分子中S-Cl键是极性共价键; S-S键是非极性共价键.每个原子都都满足8电子稳定结构。正确。D.二者都是分子晶体,通过分子间作用力结合。分子间作用力越大,克服分子间作用力使物质融化或汽化消耗的能量就越高,熔沸点就越高。故S2C12沸点比S2Br2高是因为S2C12的分子间作用力比S2Br2的大。错误。2C12的结构、性质等的知识。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目