题目内容
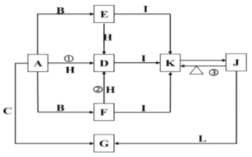
【题目】硅酸钠被国家列为“我国优先发展的精细化学品”和“今后我国无机化工产品发展重点”之一。下图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:

(1)要将洗出液中的溶质析出,采用的方法是_________。
A.蒸发结晶 B.冷却结晶
C.先蒸发,再冷却结晶 D.先冷却,再蒸发结晶
(2)在以上流程中,要将洗净的石英砂研磨成粉末,目的是_____________________________。
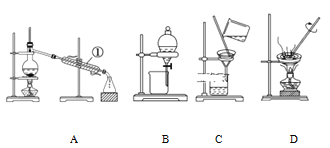
(3)蒸发时用到的硅酸盐仪器有____________________________________________________。
(4)上述流程中加入NaOH溶液,反应的离子方程式是_______________________________。
(5)硅酸钠溶液呈____性,硅酸钠的用途很广,其中的一种用途是_______________________。
(6)将用上流程中的残渣来焊接铁轨,反应的化学方程式是___________________。
【答案】A 增加反应物之间的接触面积,增大反应速率,提高生产效率。 蒸发皿、玻璃棒、酒精灯 SiO2 + 2OH— =SiO32— + H2O 碱性 作黏合剂或防腐剂或防火剂或作制皂填料或制合成洗涤剂或用于制备硅胶、分子筛等 Fe2O3 + 2Al![]() 2Fe + Al2O3
2Fe + Al2O3
【解析】
(1)石英砂(含氯化钠、氧化铁等杂质)用水洗涤得到的洗出液主要是氯化钠溶液,氯化钠溶解度随温度变化不大,可以利用蒸发结晶的方法得到溶质;冷却结晶适用于溶解度随温度变化大的物质,BCD不符合,故答案为:A.
(2)将洗净的石英砂研磨成粉末是增大接触面积,加快反应速率,提高生产效率;
(3)蒸发时用到的硅酸盐仪器主要有蒸发皿,酒精灯,玻璃棒;
(4)上流程中加入NaOH溶液是为了溶解二氧化硅除去杂质,反应的离子方程式:SiO2+2OH-=SiO32-+H2O;
(5)硅酸钠溶液呈碱性是因为硅酸根离子水解生成硅酸和氢氧根离子,反应的离子方程式为:SiO32-+2H2O![]() H2SiO3+2OH-;硅酸钠的用途很广,其中的一种用途是作黏合剂或防腐剂或合成洗涤剂或制备硅胶或分子筛等;
H2SiO3+2OH-;硅酸钠的用途很广,其中的一种用途是作黏合剂或防腐剂或合成洗涤剂或制备硅胶或分子筛等;
(6)流程中的残渣是Fe2O3,用来焊接铁轨的反应原理是利用铝热反应,反应的化学方程式 为:Fe2O3 + 2Al![]() 2Fe + Al2O3。
2Fe + Al2O3。

 阅读快车系列答案
阅读快车系列答案【题目】对于易燃、易爆、有毒的 化学物质,往往会在其包装上贴上危险警告标签.下面所 列的物质中,标签贴错了的是
选项 | A | B | C | D |
物质的化学式 | 氢氧化钠 | 金属汞 | 四氯化碳 | 烟花爆竹 |
危险警告标签 |
|
|
|
|
A. A B. B C. C D. D