题目内容
(7分) 铜和浓硫酸发生反应的化学方程式为:
Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(1)浓H2SO4作_________剂,具有 性。
(2)在该反应中,若消耗了32 g Cu,则转移了_______mol 电子 ,还原了 mol H2SO4,生成 L SO2(标准状况)气体。
(3)以下三种物质的氧化性由强到弱的顺序为: (写出序号)
① 浓H2SO4 ②稀H2SO4 ③CuSO4
【答案】
(1)氧化,氧化, (2)1 0.5 11.2 (3)①>③>②
【解析】略

练习册系列答案
相关题目
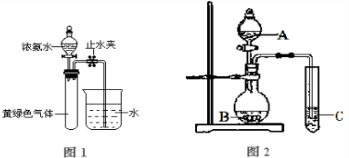


 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O