题目内容
铅蓄电池放电时发生变化:Pb+SO42--2e-=PbSO4,正极PbO2+4H++SO42-+2e-=PbSO4+2H2O,使用该电池电解AgNO3溶液时(电极材料为碳棒),若析出银10.8g时,那么电池中内耗的硫酸是( )
| A.0.05mol | B.0.10mol | C.0.25mol | D.0.5mol |
B
正确答案:B
由关系式:2Ag~2e-~2H2S04 ,现析出的Ag为10.8g/108g/mol=0.1mol,则消耗的H2SO4为0.1mol

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
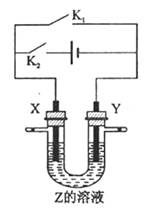
 移向Y极
移向Y极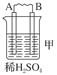


 被完全吸收,制得有较强杀菌能力的消毒液(“84消毒液”),设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是
被完全吸收,制得有较强杀菌能力的消毒液(“84消毒液”),设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是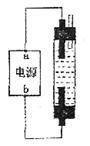
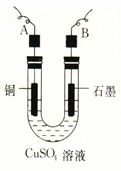
 电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如下图所示,回答下列问题:
电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如下图所示,回答下列问题: