题目内容
下列说法中,正确的是( )
| A.ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| B.ⅥA族元素的氢化物中,最稳定的氢化物常温时为无色液体 |
| C.某主族元素X的气态氢化物化学式为HX,则其最高正价为+7价 |
| D.金属元素的原子只有还原性,金属阳离子只有氧化性 |
B
第ⅠA族元素中的氢是非金属元素,A项错误;ⅥA族元素的氢化物中,H2O是最稳定的,在常温下为无色液体,B项正确;F元素的氢化物的化学式为HF,但F无正价,C项错误;Fe2+具有还原性,D项错误。

练习册系列答案
相关题目
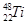 和
和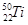 的说法中正确的是( )
的说法中正确的是( )
