题目内容
【题目】NaNO2可将正常的血红蛋白中的二价铁变为高铁血红蛋白中的三价铁,失去携氧能力。完成下列填空:
(1)N元素在元素周期表中位于第____族,N原子最外层的电子排布式是______________。
(2)Na、N、O三种元素形成的简单离子中,离子半径最小的是_______(用离子符号表示)。
(3)某工厂的废液中含有2%~5%的NaNO2直接排放会造成污染。下列试剂中,能使NaNO2转化为N2的是______________(选填编号)。
a.NaCl b.NH4Cl c.HNO3 d.H2SO4
(4)已知NaNO2能发生如下反应:NaNO2 + HI → NO↑+ I2 + NaI + H2O
①配平反应物的系数并标出电子转移的方向和数目____NaNO2 +____ HI
②当有0.75mol HI被氧化时,在标准状况下产生气体的体积是_______L。
(5)NaNO2外观与食盐相似,根据上述反应,可用于鉴别NaNO2和NaCl。现有 ①白酒、②碘化钾淀粉试纸、③淀粉、④白糖、⑤白醋,其中可选用的物质至少有______(选填编号)。
【答案】 VA 2s22p3 Na+ b 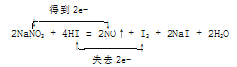 16.8 ②⑤
16.8 ②⑤
【解析】
(1)N是7号元素,最外层电子数是5,所以在元素周期表中N元素位于第二周期VA族;核外电子排布是1s22s22p3, 所以最外层电子排布式为2s22p3;
(2)Na、N、O三种元素形成的简单离子中,Na+、N3-、O2-中它们的电子层结构相同,随核电荷数递增,离子半径依次减小,所以离子半径最小的是Na+;
(3)NaNO2中的N元素的化合价是+3价,使NaNO2中的氮转化为对空气无污染的气体(氮气),需要另一种反应物具有强还原性,而且含有N元素,二者发生氧化还原反应产生N2,就不会引起环境污染,a中的Cl-只有弱还原性,a错误,b中NH4+的N元素是-3价,具有强还原性,能够与+3价的N元素发生氧化还原反应生成N2,b正确;HNO3中的N元素+5价,具有强氧化性,不符合条件,c错误;d中浓硫酸具有强氧化性,且没有N元素,也不符合条件,d错误,正确答案是b;
(4)①2I-被氧化为I2,失去2e-,NaNO2→ NO,N元素得到e-,被还原,根据电子守恒及原子守恒可得2NaNO2 + 4HI = 2NO↑+ I2 + 2NaI + 2H2O,2molHI中I失去2mol电子给NaNO2中的N,电子转移总数是2e-即:
②根据方程式2NaNO2 + 4HI = 2NO↑+ I2 + 2NaI + 2H2O可知:4molHI参加反应,有2mol被氧化,生成2mol的NO气体,所以当有0.75mol HI被氧化时,有0.75mol的NO生成,V(NO)=0.75mol×22.4L·mol-1=16.8L;
(5)鉴别亚硝酸钠和氯化钠固体,利用题干中给的信息: NaNO2能够将HI氧化为I2,I2遇淀粉溶液变为蓝色,而NaCl没有该性质,所以利用上述反应可以鉴别NaNO2和NaCl的物质有:②碘化钾淀粉试纸、⑤白醋,,答案选②⑤。

 阅读快车系列答案
阅读快车系列答案