题目内容
下列有关溶液配制的叙述正确的是
A.将58.5g NaCl溶于1L水中可得1L 1.00mol·L-1 NaCl溶液
B.溶液定容时仰视容量瓶的刻度线,所得溶液的浓度偏大
C.定容摇匀后发现液面低于刻度线,需再加水至刻度线
D.容量瓶中原有少量的蒸馏水,不影响配制溶液的浓度
D
【解析】
试题分析:A.将58.5g NaCl溶于1L水中得到的溶液体积不一定是1L,所以浓度也就不一定是1.00mol·L-1 NaCl溶液。错误。B. 溶液定容时仰视容量瓶的刻度线,则溶液的体积偏大,由于溶质的物质的量不变,所以所得溶液的浓度偏小。错误。C.定容摇匀时一部分溶液粘在容量瓶的瓶颈上,致使溶液的液面低于刻度线,但由于溶液有均一性。所以后来发现液面低于刻度线,也不需要再加水至刻度线。错误。若加水会对溶液起到稀释作用使溶液的浓度降低。错误。D.容量瓶中原有少量的蒸馏水,只要溶质的物质的量不变,最后定容时液面的最低处与刻度线相切,就不影响配制溶液的浓度。正确。
考点:考查物质的量浓度的溶液的配制的误差分析等知识。

四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
| W | X | Y | Z |
结构或性质 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最低负价之和为零 |
(1)Z在元素周期表中位于 族。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是 (填元素符号)。
(3)①下列可作为比较X和Y金属性强弱的依据是 (填序号)。
A.自然界中的含量 B.单质与酸反应时失去的电子数
C.单质与水反应的难易程度 D.最高价氧化物对应水化物的碱性
②从原子结构的角度解释X的金属性强于Y的原因: ,原子半径X>Y,所以原子核对最外层电子的吸引力X<Y,失电子能力X>Y。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物的溶液混合,反应的化学方程式是 。
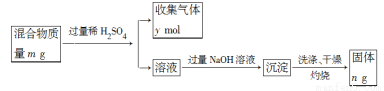
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数。能确定混合物中Y的质量分数的数据有 (填序号)。
A.m、n B.m、y C.n、y