题目内容
食盐是日常生活的必需品,也是重要的化工原料。
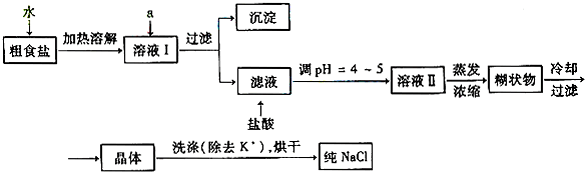
(1)粗食盐常含有少量Ca2+、Mg2+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
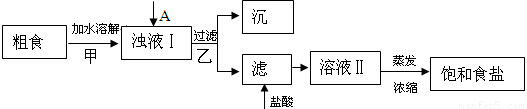
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液
(1)①欲除去浊液Ⅰ中的Ca2+、Mg2+、SO42-,选出A所代表的试剂,按滴加顺序依次为 (只填化学式),检验溶液中SO42-沉淀完全的操作为 。
②加盐酸的目的是(用离子方程式表示) 。
③上述流程中,甲、乙两个过程均要用到玻璃棒,玻璃棒的作用分别是甲 ,乙 。
(2)工业上用惰性电极电解饱和食盐水法制取盐酸,写出电解饱和食盐水的化学方程式 ;用试纸检验电解食盐水阳极产物的方法是 。
(1)①BaCl2、NaOH 、Na2CO3或NaOH、BaCl2、Na2CO3
稍待片刻,待沉淀沉降完毕,上层出现清液,向上层清液中继续滴加氯化钡溶液,无沉淀生成,则沉淀完全。
②OH-+H+=H2O CO32-+2H+=H2O+CO2↑
③搅拌引流
(2)2NaCl+2H2O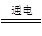 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
用湿润的蓝色石蕊试纸放在阳极区气体中,试纸先变红,后退色,证明有氯气生成(或用湿润的KI-淀粉试纸放在阳极区气体中,试纸变蓝色)
【解析】
试题分析:(1)沉淀Ca2+用Na2CO3溶液、沉淀Mg2+用NaOH溶液、沉淀SO42-用BaCl2溶液,但要注意除杂试剂必须过量且过量的试剂后续过程中需除去,所以试剂滴加的顺序是BaCl2、NaOH 、Na2CO3或NaOH、 BaCl2、Na2CO3。检验SO42-沉淀完全的操作方法为将浊液静置,向上层清液中继续滴加氯化钡溶液,无沉淀生成,说明SO42-完全沉淀;滤液中加盐酸的作用是除去过量的CO32-和OH-;溶解时用玻璃棒搅拌,加快溶解速度。过滤时用玻璃棒引流。
(2)电解饱和食盐水生成氢氧化钠、氢气和氯气;阳极产生氯气,可用湿润淀粉-KI试纸检验。
考点:化学实验 电解 元素及其化合物
点评:除杂时要注意试剂加入的顺序且所加试剂需过量,过量的试剂后续过程中需除去。

 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案