题目内容
【题目】已知 Ksp(AgCl)=1.0×10-12,Ksp(AgI)=1.0×10-16。下列说法正确的是
A.向AgCl饱和溶液中加入少量水,c(Ag+)先减小后增大
B.向0.01mol/L的AgNO3溶液中,加入等体积的浓度均为0.001mol/L的Cl-、I-的混合溶液,只析出AgI沉淀
C.常温下,AgCl沉淀若要在NaI溶液中开始转化为AgI沉淀,则NaI的浓度必须不低于1.0×10-10mol/L
D.向10ml0.1mol/L AgNO3溶液中滴加1ml0.1mol/L的NaCl溶液,有白色沉淀生成,再滴加0.1mol/L的KI溶液,有黄色沉淀生成,说明Ksp(AgCl)> Ksp(AgI)
【答案】C
【解析】
A. 向AgCl饱和溶液中加入少量水后仍然是AgCl饱和溶液,Cl-的浓度不变;
B. 溶解度小的物质先生成沉淀,溶解度大的物质后生成沉淀;
C. 根据Ksp(AgCl)求出c(Ag+),再利用Ksp(AgI)求出I-的浓度;
D. 加入的NaCl溶液和KI溶液较少,并不能证明沉淀发生了转化。
A. 向AgCl饱和溶液中加入少量水后,得到的仍然是AgCl饱和溶液,Cl-的浓度不变,A项错误;
B. 在0.01mol/L的AgNO3溶液中,加入等体积的浓度均为0.001mol/L的Cl-、I-的混合溶液,由于AgI的溶度积小,因此AgI先形成沉淀析出,并不是只析出AgI沉淀,B项错误;
C. 已知Ksp(AgCl)=1.0×10-12,那么c(Ag+)=![]() =
=![]() =1.0×10-6mol/L,c(I-)=
=1.0×10-6mol/L,c(I-)= =
=![]() =1.0×10-10mol/L,因此NaI的浓度必须不低于1.0×10-10mol/L,C项正确;
=1.0×10-10mol/L,因此NaI的浓度必须不低于1.0×10-10mol/L,C项正确;
D. 向10ml0.1mol/L AgNO3溶液中滴加1ml0.1mol/L的NaCl溶液,有白色沉淀生成,再滴加0.1mol/L的KI溶液,有黄色沉淀生成,说明生成AgI,但由于加入的NaCl溶液和KI溶液较少,并不能证明沉淀发生了转化,因此不能证明Ksp(AgCl)> Ksp(AgI),D项错误;
答案选C。

【题目】实验室模拟工业生产食品香精菠萝酯(![]() )的简易流程如图:
)的简易流程如图:
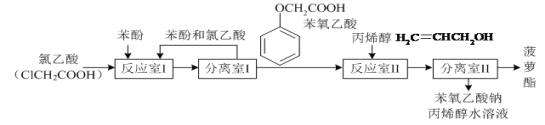
有关物质的熔、沸点如表:
苯酚 | 氯乙酸 | 苯氧乙酸 | |
熔点/℃ | 43 | 62 | 99 |
沸点/℃ | 181.9 | 189 | 285 |
试回答下列问题:
(1)反应室I中反应的最佳温度是104℃,为较好地控制温度在102℃~106℃之间,加热时可选用________(选填字母)。
A.火炉直接加热 B.水浴加热 C.油浴加热.
(2)分离室I采取的操作名称是__________。
(3)苯氧乙酸含氧官能团的名称__________。
(4)下列叙述错误的是_________。
A.反应室I产物中残留的苯酚可用FeCl3溶液检验
B.反应室Ⅱ产物中残留的丙烯醇可用溴水检验
C.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应
D.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
(5)反应室I中发生反应的化学方程式是______。
(6)分离室Ⅱ的操作为:①用NaHCO3溶液洗涤后分液;②有机层用水洗涤后分液;洗涤时不能用NaOH溶液代替NaHCO3溶液,其原因是_______(用化学方程式表示)。
【题目】某化学兴趣小组用如图所示装置制取氯酸钾、次氯酸钠和氯水并进行有关探究实验。

实验Ⅰ:制取氯酸钾、次氯酸钠和氯水
(1)写出装置A实验室制取Cl2的化学方程式______。
(2)制取实验结束后,取出装置B中试管,冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有胶头滴管、烧杯、________、________。为提高氯酸钾和次氯酸钠的产率,在实验装置中还需要改进的是__________。
(3)装置C中反应需要在冰水浴中进行,其原因是_______。
实验Ⅱ:尾气处理。实验小组利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(4)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中CO2的影响)。
①提出合理假设
假设1:只存在SO32-;
假设2:既不存在SO32-,也不存在ClO-;
假设3:________。
②设计实验方案,进行实验。请完成下列表格,写出相应的实验步骤以及预期现象和结论。限选实验试剂:3 mol· L-1 H2SO4、1 mol· L-1NaOH溶液、0.01 mol· L-1酸性KMnO4溶液、淀粉KI溶液。
实验步骤 | 预期现象和结论 |
步骤1:取少量吸收液分置于A、B试管中 | |
步骤2:向A试管中滴加0.01 mol·L-1酸性KMnO4溶液 | (1)若溶液褪色,则假设1成 |
(2)若溶液不褪色,则假设2或3成立 | |
步骤3:__________ | _________ |
_________ |