题目内容
【题目】下表是元素周期表的一部分:(不得用a~h字母回答)元素周期表有7个横行,每一个横行称为“周期”,周期序数=电子层数;元素周期表共有18列,每一列称为 “族”,下表中的7列为主族元素,分别用罗马数字Ⅰ、Ⅱ、……表明族序数,族序数=最外层电子数。

根据a~h各元素的性质,选择相应的化学符号、化学式或化学方程式填空:
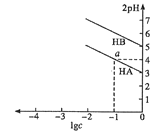
(1)单质氧化性最强的是__________,酸性最强的含氧酸是_____________。
(2)写出e的碱性气态氢化物的电子式_____,将它和化合物df 2通入饱和食盐水发生反应的化学方程式是_____。
(3)最高价氧化物对应的水化物中,碱性最强的是___________。
(4)在b、c、g、h中,常见离子半径最大的是__________。
【答案】F2 HClO4 ![]() NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl NaOH Cl-
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl NaOH Cl-
【解析】
根据周期表的结构分析,a为氢,b为钠,c为铝,d为碳,e为氮,f为氧,g为氟,h为氯。
(1)单质氧化性最强的为氟气,F2;酸性最强的含氧酸为HClO4;
(2)氮的碱性气态氢化物为氨气,电子式为![]() ;和二氧化碳通入饱和食盐水中的方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
;和二氧化碳通入饱和食盐水中的方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
(3)最高价氧化物对应的水化物中碱性最强的为氢氧化钠NaOH。
(4)钠离子,铝离子,氟离子,和氯离子中根据电子层数越多,半径越大分析,氯离子半径最大。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】已知1L无色待测液中除含有0.2mo/L的Na+外,还可能含下列离子中的一种或几种:
阳离子 | K+、NH4+、Ca2+、Ba2+、Fe3+ |
阴离子 | Cl-、Br-、CO32-、HCO3-、SO42- |
现进行如图实验操作(每次实验所加试剂均过量)
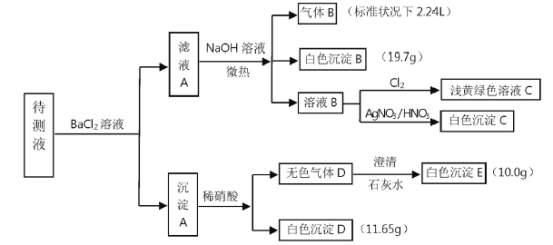
(1)由气体B可确定待测液中含有的离子是___________。
(2)由白色沉淀D和白色沉淀E可以判定待测液中一定含有的离子是___________,据此可以确定待液中一定不存在的离子是___________。
(3)由白色沉淀B可确定待测液中含有的离子是___________。
(4)某同学认为待液中一定不含溴离子,判断的依据是______________________。
(5)综上分析,待测液中K+的最小浓度为___________。
【题目】根据下列实验事实得出的相应结论正确的是( )
选项 | 实验事实 | 结论 |
A | NH3 的水溶液可以导电 | NH3 是电解质 |
B | SO2 通入硝酸钡溶液出现白色沉淀 | BaSO3 不溶于强酸 |
C | 浓硝酸久置发黄 | 硝酸不稳定 |
D | 浓硫酸能脱去胆矾晶体中的水 | 浓硫酸具有脱水性 |
A.AB.BC.CD.D