题目内容
【题目】氢氧燃料电池构造如图所示。其电池反应方程式为: 2H2+O2=2H2O,下列说法不正确的是
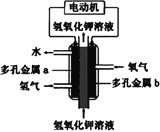
A. 多孔金属a作负极
B. 多孔金属b上,发生还原反应
C. 电池工作时,电解质溶液中OH移向a极
D. 正极的电极反应为:O2+4e+4H+=2H2O
【答案】D
【解析】
氢氧碱性燃料电池中,通入氢气的一极为电源的负极a,发生氧化反应,电极反应式为H2-2e-+2OH-=2H2O,通入氧气的一极为原电池的正极,b电极反应式为O2+4e-+2H2O=4OH-,原电池工作时,电子由负极a经外电路流向正极b,内电路中阳离子移向正极b、阴离子移向负极a,据此解答。
A.氢氧碱性燃料电池中,通入氢气的一极失去电子、发生氧化反应,为电源的负极,即多孔金属a作负极,故A正确;
B.通入氧气的一极为原电池的正极,O2在正极b上得到电子、被还原,故B正确;
C.原电池工作时,内电路中阳离子移向正极b、阴离子移向负极a,即电解质溶液中OH-移向a极,故C正确;
D.碱性条件下,在电极方程式的书写中不会出现H+,正极b电极反应式为O2+4e-+2H2O=4OH-,故D错误;答案为D。

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目