题目内容
某溶液中含有K+、Mg2+、Al3+、Cu2+等离子,为了将它们一一分离(不要求各离子恢复到原来的形态),某同学设计了如下四个实验方案,其中不正确的是[已知:Mg2+、Al3+溶液中通入H2S不产生沉淀;Ksp(CuS )=1.3×10-36.]
- A.试液
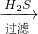 滤液
滤液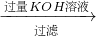 滤液
滤液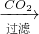

- B.试液
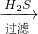 滤液
滤液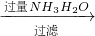 沉淀
沉淀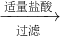

- C.

- D.

B
分析:通入H2S可的到CuS沉淀,加入过量KOH,生成AlO2-,通入过量二氧化碳气体生成Al(OH)3沉淀,加入过量氨水Cu(OH)2溶解,Mg2+、Al3+与碳酸根离子发生互促水解生成Mg(OH)2和Al(OH)3,以此解答该题.
解答:A.通入H2S可的到CuS沉淀,加入过量KOH得到Mg(OH)2沉淀,过滤后在溶液中通入过量二氧化碳气体生成Al(OH)3沉淀,K+存在与滤液中,故A正确;
B.通入H2S可的到CuS沉淀,加入过量氨水生成Mg(OH)2和Al(OH)3,加入盐酸沉淀溶解又生成Mg2+、Al3+,不能分离,故B错误;
C.通入H2S可的到CuS沉淀,滤液中加入过量碳酸钾溶液生成Mg(OH)2和Al(OH)3,加入过滤KOH溶解Al(OH)3,过滤后通入过量二氧化碳气体生成Al(OH)3沉淀,K+存在与滤液中,故C正确;
D.加入过量KOH得到Mg(OH)2和Cu(OH)2,加入过量氨水Cu(OH)2溶解,可分离Mg(OH)2和Cu(OH)2,过滤后在溶液中通入过量二氧化碳气体生成Al(OH)3沉淀,K+存在与滤液中,故D正确.
故选B.
点评:本题考查物质的分离、提出的实验方案的评价,题目难度中等,注意把握相关物质的性质,为解答该题的关键.
分析:通入H2S可的到CuS沉淀,加入过量KOH,生成AlO2-,通入过量二氧化碳气体生成Al(OH)3沉淀,加入过量氨水Cu(OH)2溶解,Mg2+、Al3+与碳酸根离子发生互促水解生成Mg(OH)2和Al(OH)3,以此解答该题.
解答:A.通入H2S可的到CuS沉淀,加入过量KOH得到Mg(OH)2沉淀,过滤后在溶液中通入过量二氧化碳气体生成Al(OH)3沉淀,K+存在与滤液中,故A正确;
B.通入H2S可的到CuS沉淀,加入过量氨水生成Mg(OH)2和Al(OH)3,加入盐酸沉淀溶解又生成Mg2+、Al3+,不能分离,故B错误;
C.通入H2S可的到CuS沉淀,滤液中加入过量碳酸钾溶液生成Mg(OH)2和Al(OH)3,加入过滤KOH溶解Al(OH)3,过滤后通入过量二氧化碳气体生成Al(OH)3沉淀,K+存在与滤液中,故C正确;
D.加入过量KOH得到Mg(OH)2和Cu(OH)2,加入过量氨水Cu(OH)2溶解,可分离Mg(OH)2和Cu(OH)2,过滤后在溶液中通入过量二氧化碳气体生成Al(OH)3沉淀,K+存在与滤液中,故D正确.
故选B.
点评:本题考查物质的分离、提出的实验方案的评价,题目难度中等,注意把握相关物质的性质,为解答该题的关键.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
某溶液中含有Cl-、SO
、Fe3+、K+、M,且离子的物质的量之比为2:3:1:3:1,则微粒M为( )
2- 4 |
| A、Na+ |
| B、S2- |
| C、Mg2+ |
| D、Ba2+ |
现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
T |
M层上电子数是K层上电子数的3倍 |
|
X |
最外层电子数是次外层电子数的2倍 |
|
Y |
常温下单质为双原子分子,其氢化物水溶液呈碱性 |
|
Z |
元素最高正价是+7价 |
(1)元素X位于元素周期表的第______________周期第________族,它的一种核素可测定文物年代,这种核素的符号是________。
(2)元素Y的原子结构示意图为______________,与氢元素形成一种离子YH,写出某溶液中含有该微粒的检验方法___________________________________________________。
(3)元素Z与元素T相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下Z的单质和T的单质状态不同 b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应