题目内容
标准状况下,mg气体A与ng气体B所含分子数相同,下列说法不正确的是
- A.A与B相对分子质量之比为m:n
- B.同质量的A与B所含分子数之比为n:m
- C.相同状况下,同体积的A与B的质量之比为m:n
- D.标准状况下,A与B的密度之比为n:m
D
分析:标准状况下,分子数相同的气体A和B,它们的物质的量相同,则相对分子质量之比、同体积的气体的体积之比均等于质量之比、分子数之比与物质的摩尔质量成反比,由ρ=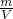 来分析密度之比.
来分析密度之比.
解答:A、由n= 可知,分子数相同的气体,相对分子质量之比等于质量之比,即A与B相对分子质量之比为mg:ng=m:n,故A正确;
可知,分子数相同的气体,相对分子质量之比等于质量之比,即A与B相对分子质量之比为mg:ng=m:n,故A正确;
B、A与B相对分子质量之比为m:n,同质量时由n= 可知,分子数之比等于
可知,分子数之比等于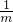 :
: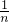 =n:m,故B正确;
=n:m,故B正确;
C、相同状况下,同体积的A与B的物质的量相同,则质量之比等于相对分子质量之比,即为m:n,故C正确;
D、标准状况下,Vm相同,由ρ=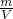 可知,密度之比等于摩尔质量之比等于相对分子质量之比,即为m:n,故D不正确;
可知,密度之比等于摩尔质量之比等于相对分子质量之比,即为m:n,故D不正确;
故选D.
点评:本题考查阿伏伽德罗定律及其推论,明确同温、同压、同体积,则气体的分子数相同、物质的量相同及质量、物质的量、摩尔质量的关系是解答的关键.
分析:标准状况下,分子数相同的气体A和B,它们的物质的量相同,则相对分子质量之比、同体积的气体的体积之比均等于质量之比、分子数之比与物质的摩尔质量成反比,由ρ=
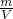 来分析密度之比.
来分析密度之比.解答:A、由n=
 可知,分子数相同的气体,相对分子质量之比等于质量之比,即A与B相对分子质量之比为mg:ng=m:n,故A正确;
可知,分子数相同的气体,相对分子质量之比等于质量之比,即A与B相对分子质量之比为mg:ng=m:n,故A正确;B、A与B相对分子质量之比为m:n,同质量时由n=
 可知,分子数之比等于
可知,分子数之比等于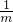 :
: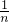 =n:m,故B正确;
=n:m,故B正确;C、相同状况下,同体积的A与B的物质的量相同,则质量之比等于相对分子质量之比,即为m:n,故C正确;
D、标准状况下,Vm相同,由ρ=
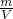 可知,密度之比等于摩尔质量之比等于相对分子质量之比,即为m:n,故D不正确;
可知,密度之比等于摩尔质量之比等于相对分子质量之比,即为m:n,故D不正确;故选D.
点评:本题考查阿伏伽德罗定律及其推论,明确同温、同压、同体积,则气体的分子数相同、物质的量相同及质量、物质的量、摩尔质量的关系是解答的关键.

练习册系列答案
相关题目