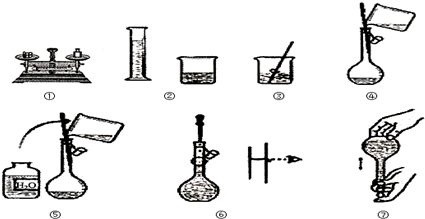
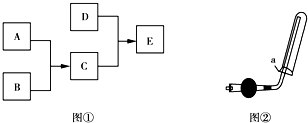
��Ŀ����
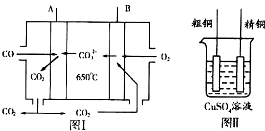 ͭ���仯����������������й㷺Ӧ�ã���ش��������⣺
ͭ���仯����������������й㷺Ӧ�ã���ش��������⣺��1����Ȼ��ر���ԭ��ͭ�����ᆳ�������������ú���CuSO4��Һ�������������������ܵ�ZnS������ת��Ϊͭ����CuS����д��CuSO4ת��Ϊͭ�������ӷ���ʽ
��2����ҵ���Ի�ͭ��CuFeS2��Ϊԭ�ϣ����û�������������ͭ���м���̻ᷢ����Ӧ��2Cu2O+Cu2S
| ||
��3��ͼ����һ������ȼ�ϵ�أ�����COΪȼ�ϣ�һ��������Li2CO3��Na2CO3���ڻ����Ϊ����ʣ�ͼ���Ǵ�ͭ������װ��ͼ��������ȼ�ϵ��Ϊ��Դ���д�ͭ�ľ���ʵ�飮
��д��A���ĵ缫��Ӧʽ
��Ҫ��ȼ�ϵ��Ϊ��Դ���д�ͭ�ľ���ʵ�飬��ͭ��Ӧ��
��4������һ����Ca2+��Cu2+�Ļ����Һ�еμ�Na2CO3��Һ������������CuCO3���������ݸ�ʵ��ɵó��Ľ�����
A��KSP��CuCO3����KSP��CaCO3�� B��c��Cu2+����c��Ca2+��
C��
| c(Cu2+) |
| c(Ca2+) |
| KSP(CuCO3) |
| KSP(CaCO3) |
| c(Cu2+) |
| c(Ca2+) |
| KSP(CuCO3) |
| KSP(CaCO3) |
���㣺��ѧ��Դ���͵��,������ԭ��Ӧ,���ܵ���ʵ��ܽ�ƽ�⼰����ת���ı���,���ԭ��
ר�⣺�����������������,Ԫ�ؼ��仯����
��������2�����ܵ���ʵ��ܽ�ƽ�⼰����ת�����ܽ�ȴ���������ܽ��С������ת����
��2������Ԫ�صĻ��ϼ۱仯�жϣ��õ��ӻ��ϼ۽��͵���������������SO2����Ư���ԣ���ʹƷ����Һ��ɫ�����Ȼָ�ԭɫ��
��3����ԭ��ظ�������������Ӧ������������ԭ��Ӧ������ͨ��������һ��Ϊ������ͨ��CO��һ��Ϊ������
�ڴ�ͭ����ʱ����ͭ�����������Դ��������������ͭ�е�Au��Ag�������ڵ����е��·����Ե�����ʽ�����������·���Fe��Fe2+����ʽ������Һ�У�
�۸��ݵ��ӵ�ʧ�غ��Լ���ͭ��ͭ���ӵõ����������㣻
��4��������CuCO3������˵����Һ��ͭ��������̼��ͭ������Ҫ��̼�������Ũ��
С�ڸ���������̼��Ƴ�����Ҫ��̼�������Ũ��
���ݴ˽��н��
��2������Ԫ�صĻ��ϼ۱仯�жϣ��õ��ӻ��ϼ۽��͵���������������SO2����Ư���ԣ���ʹƷ����Һ��ɫ�����Ȼָ�ԭɫ��
��3����ԭ��ظ�������������Ӧ������������ԭ��Ӧ������ͨ��������һ��Ϊ������ͨ��CO��һ��Ϊ������
�ڴ�ͭ����ʱ����ͭ�����������Դ��������������ͭ�е�Au��Ag�������ڵ����е��·����Ե�����ʽ�����������·���Fe��Fe2+����ʽ������Һ�У�
�۸��ݵ��ӵ�ʧ�غ��Լ���ͭ��ͭ���ӵõ����������㣻
��4��������CuCO3������˵����Һ��ͭ��������̼��ͭ������Ҫ��̼�������Ũ��
| Ksp(CuCO3) |
| c(Cu2+) |
| Ksp(CaCO 3) |
| c(Ca2+) |
���
�⣺��1��ZnS���ܽ��С��ͭ����CuS����CuSO4ת��Ϊͭ�������ӷ���ʽ��Cu2++ZnS=CuS+Zn2+���ʴ�Ϊ��Cu2++ZnS=CuS+Zn2+��
��2��2Cu2O+Cu2S
6Cu+SO2�����÷�Ӧ��ͭ�Ļ��ϼ���+1�۱�Ϊ0�ۣ�ͭԪ���ڸ÷�Ӧ�еõ��ӻ��ϼ۽��ͣ����Ը÷�Ӧ�е���������Cu2O��Cu2S��
�ʴ�Ϊ��Cu2O��Cu2S��
��3��SO2����Ư���ԣ���ʹƷ����Һ��ɫ�����Ȼָ�ԭɫ�����Խ�����ͨ��Ʒ����Һ��Һ��ɫ�����Ȼָ�ԭɫ��
�ʴ�Ϊ��������ͨ��Ʒ����Һ��Һ��ɫ�����Ȼָ�ԭɫ��
��3����CO���л�ԭ�ԣ��ڸ����Ϸ���������Ӧ����CO2���缫��ӦʽΪ��CO-2e-+CO32-�T2CO2��
�ʴ�Ϊ��CO-2e-+CO32-=2CO2��
����AΪ������BΪ��������ͭ����ʱ����ͭ�����������Դ������B������Au��Ag�Ƚ��ȶ�������Ӧ���Ե�����ʽ������c���������·���Feʧȥ���ӱ��Fe2+����ʽ������Һ�У�
�ʴ�Ϊ��B�� Au��Ag�Ե�����ʽ�����������·���Fe��Fe2+����ʽ������Һ�У�
�۵����ı�״����1.12L COʱ���缫��Ӧʽ��CO-2e-+CO32-=2CO2��ʧȥ����Ϊ
��2=0.1mol����ͭ�缫�缫��Ӧʽ��Cu2++2e-=Cu���ɵ��ӵ�ʧ�غ��֪Cu2+�����ʵ���Ϊ
=0.05mol����ͭ�缫���������ӵ�����Ϊ��0.05mol��64g/mol=3.2g��
�ʴ𰸣�����3.2g��
��4��̼��ͭ��̼��Ƶ��ܶȻ��ֱ�Ϊ��Ksp��CuCO3��=c��Cu2+��?c��CO32-����Ksp��CaCO3��=c��Ca2+��?c��CO32-������һ����Ca2+��Cu2+�Ļ����Һ�еμ�Na2CO3��Һ������������CuCO3������˵��ͭ��������̼��ͭ������Ҫ��̼�������Ũ��С�ڸ���������̼��Ƴ�����Ҫ��̼������ӣ���
��
�������ã�
��
��
�ʴ�Ϊ��C��
��2��2Cu2O+Cu2S
| ||
�ʴ�Ϊ��Cu2O��Cu2S��
��3��SO2����Ư���ԣ���ʹƷ����Һ��ɫ�����Ȼָ�ԭɫ�����Խ�����ͨ��Ʒ����Һ��Һ��ɫ�����Ȼָ�ԭɫ��
�ʴ�Ϊ��������ͨ��Ʒ����Һ��Һ��ɫ�����Ȼָ�ԭɫ��
��3����CO���л�ԭ�ԣ��ڸ����Ϸ���������Ӧ����CO2���缫��ӦʽΪ��CO-2e-+CO32-�T2CO2��
�ʴ�Ϊ��CO-2e-+CO32-=2CO2��
����AΪ������BΪ��������ͭ����ʱ����ͭ�����������Դ������B������Au��Ag�Ƚ��ȶ�������Ӧ���Ե�����ʽ������c���������·���Feʧȥ���ӱ��Fe2+����ʽ������Һ�У�
�ʴ�Ϊ��B�� Au��Ag�Ե�����ʽ�����������·���Fe��Fe2+����ʽ������Һ�У�
�۵����ı�״����1.12L COʱ���缫��Ӧʽ��CO-2e-+CO32-=2CO2��ʧȥ����Ϊ
| 1.12L |
| 22.4L/mol |
| 0.1mol |
| 2 |
�ʴ𰸣�����3.2g��
��4��̼��ͭ��̼��Ƶ��ܶȻ��ֱ�Ϊ��Ksp��CuCO3��=c��Cu2+��?c��CO32-����Ksp��CaCO3��=c��Ca2+��?c��CO32-������һ����Ca2+��Cu2+�Ļ����Һ�еμ�Na2CO3��Һ������������CuCO3������˵��ͭ��������̼��ͭ������Ҫ��̼�������Ũ��С�ڸ���������̼��Ƴ�����Ҫ��̼������ӣ���
| Ksp(CuCO3) |
| c(Cu2+) |
| Ksp(CaCO3) |
| c(Ca2+) |
| c(Cu2+) |
| c(Ca2+) |
| Ksp(CuCO3) |
| Ksp(CaCO3) |
�ʴ�Ϊ��C��
���������⿼��ͭ���仯��������ʣ��漰������ԭ��Ӧ�������ԭ����ԭ���ԭ�����ܶȻ��ļ��㣬�Ѷ��Դ�

��ϰ��ϵ�д�
 �����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д� Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д� �����������ҵ�������������ϵ�д�
�����������ҵ�������������ϵ�д�
�����Ŀ
��ѧ���������ճ�������������Ҫ��Ӧ�ã�����˵������ȷ���ǣ�������
| A���̬���ʲ������ľ�һ��ʩ�� |
| B���Ҵ���ͨ�����۵�����ԭ�Ϸ����Ƶã����ڿ�������Դ |
| C��������ά���ϳ���ά��������ά���ά�����л��߷��ӻ����� |
| D��MgO���۵�ܸߣ��������������²��ϣ�����ҵ�ϲ���MgO��þ |
����װ�û�����ܴﵽʵ��Ŀ���ǣ�������
A��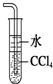 ����NH3 |
B��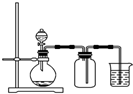 ��ͭƬ��ϡ������NO |
C��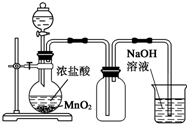 ʵ������Cl2��β���������� |
D��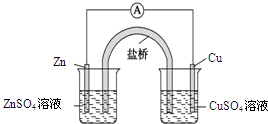 ����ͭпԭ��أ����ŵ����ã���ʹ���ձ�����Һ��ͨ�� |
�����������Ͷ��������������ݵķ����ǣ�������
| A���۲���ɫ |
| B���ø����Ʒ����ֽ |
| C����ʪ�����ɫ��̪��ֽ |
| D��ͨ�����ʯ��ˮ |