题目内容
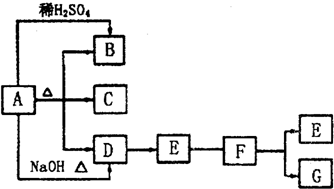
下列A~G均是中学常见化合物,它们之间有如图的转化关系(部分反应物或生成物略去),已知B为一种气体,E、F、G三种化合物中均含有同一种元素M,且价态互不相同.请回答下列问题.
(1)M元素为 .
(2)B是 或 ,写出两种鉴别它们的方法 ; .
(3)若A与G反应也能制B,且反应中n(A):n(G)=1:2,则此时该反应的离子方程式是 .
(4)若B与F在一定条件下反应生成一种化合物和一种单质,该反应的化学方程式为 .

(1)M元素为
(2)B是
(3)若A与G反应也能制B,且反应中n(A):n(G)=1:2,则此时该反应的离子方程式是
(4)若B与F在一定条件下反应生成一种化合物和一种单质,该反应的化学方程式为
分析:A能分解生成至少三种产物,反应主要是碳酸氢盐、亚硫酸氢盐、铵盐的分解,E、F、G是含有M元素的价态不同的三种化合物,符合该条件的元素只有N元素,NO2溶于水能实现F、E、G之间的转化,可推知A为铵盐、结合B为气体可知A为(NH4)2SO3或NH4HSO3或(NH4)2CO3或NH4HCO3,结合转化关系可知,B为SO2或CO2,C为H2O,D为NH3,E为NO,F为NO2,G为HNO3,据此解答.
解答:解:A能分解生成至少三种产物,反应主要是碳酸氢盐、亚硫酸氢盐、铵盐的分解,E、F、G是含有M元素的价态不同的三种化合物,符合该条件的元素只有N元素,NO2溶于水能实现F、E、G之间的转化,可推知A为铵盐、结合B为气体可知A为(NH4)2SO3或NH4HSO3或(NH4)2CO3或NH4HCO3,结合转化关系可知,B为SO2或CO2,C为H2O,D为NH3,E为NO,F为NO2,G为HNO3,
(1)由上述分析可知,M为氮元素,故答案为:氮;
(2)由上述分析可知,B为SO2或CO2,将B通入品红溶液,如溶液退色,则为SO2,如不退色,则为CO2;将B通入酸性KMnO4溶液中,如褪色,则为SO2,如不褪色,则为CO2;
故答案为:SO2 CO2;将B通入品红溶液,如溶液退色,则为SO2,如不退色,则为CO2;将B通入酸性KMnO4溶液中,如褪色,则为SO2,如不褪色,则为CO2;
(3)若A与G反应也能制B,且反应中n(A):n(G)=1:2,则A为(NH4)2CO3,反应离子方程式为:2H++CO32-═CO2↑+H2O,
故答案为:2H++CO32-═CO2↑+H2O;
(4)若B与F在一定条件下反应生成一种化合物和一种单质,则生成氮气与三氧化硫,所以反应的化学方程式为:2NO2+4SO2═N2+4SO3,
故答案为:2NO2+4SO2═N2+4SO3.
(1)由上述分析可知,M为氮元素,故答案为:氮;
(2)由上述分析可知,B为SO2或CO2,将B通入品红溶液,如溶液退色,则为SO2,如不退色,则为CO2;将B通入酸性KMnO4溶液中,如褪色,则为SO2,如不褪色,则为CO2;
故答案为:SO2 CO2;将B通入品红溶液,如溶液退色,则为SO2,如不退色,则为CO2;将B通入酸性KMnO4溶液中,如褪色,则为SO2,如不褪色,则为CO2;
(3)若A与G反应也能制B,且反应中n(A):n(G)=1:2,则A为(NH4)2CO3,反应离子方程式为:2H++CO32-═CO2↑+H2O,
故答案为:2H++CO32-═CO2↑+H2O;
(4)若B与F在一定条件下反应生成一种化合物和一种单质,则生成氮气与三氧化硫,所以反应的化学方程式为:2NO2+4SO2═N2+4SO3,
故答案为:2NO2+4SO2═N2+4SO3.
点评:本题主要考查无机物推断、元素及化合物之间的转化关系,本题的突破点隐蔽,题目开放性、综合性较强,重点考查学生能否根据题中的信息,结合掌握的元素及化合物的性质进行推理分析,难度较大.(3)(4)为易错点,学生容易审题不清写成SO32-与H+的反应,不能联系氧化还原原理,造成无法答题.

练习册系列答案
相关题目