题目内容
【题目】高血脂是一种常见的心血管疾病,治疗高血脂的新药I的合成路线如下:

已知:
回答下列问题:
(1)反应①所需试剂、条件分别是____________;F 的化学名称为____________。
(2)②的反应类型是______________;A→B 的化学方程式为_________________。
(3)G 的结构简式为______________;H 中所含官能团的名称是____________。
(4)化合物W 的相对分子质量比化合物C 大14,且满足下列条件,W 的可能结构有__种。
①遇FeCl3 溶液显紫色②属于芳香族化合物③能发生银镜反应其中核磁共振氢谱显示有5 种不同化学环境的氢,峰面积比为2:2:2:1:1,写出符合要求的W 的结构简式____________。
(5)设计用甲苯和乙醛为原料制备 的合成路线,其他无机试剂任选(合成路线常用的表示方式为:
的合成路线,其他无机试剂任选(合成路线常用的表示方式为: )____________。
)____________。
【答案】Cl2、光照 辛醛 取代反应 ![]()
 羟基 13
羟基 13 ![]()

【解析】
根据流程可知A为![]() ,B为
,B为![]() ,C为
,C为 ,E为HCHO,G为
,E为HCHO,G为 。
。
甲苯→ ,发生的是取代反应,所需试剂、条件分别是Cl2、光照;F为
,发生的是取代反应,所需试剂、条件分别是Cl2、光照;F为![]() ,化学名称为辛醛,故答案为:Cl2、光照;辛醛。
,化学名称为辛醛,故答案为:Cl2、光照;辛醛。
(2)反应②是C和H发生的酸和醇的酯化反应(取代反应),A→B 的化学方程式为
![]() ,故答案为:
,故答案为:
取代反应;![]() 。
。
(3)G 的结构简式为 ;G→H,是-CHO和H2的加成反应,所以H 中所含官能团的名称是羟基,故答案为:
;G→H,是-CHO和H2的加成反应,所以H 中所含官能团的名称是羟基,故答案为: ;羟基。
;羟基。
(4)C为 ,化合物W 的相对分子质量比化合物C 大14,W比C多一个CH2,遇FeCl3 溶液显紫色含有酚羟基,属于芳香族化合物含有苯环,能发生银镜反应含有醛基,第一种情况是苯环上放三种基团,醛基、羟基和甲基,先固定醛基和羟基的位置,邻间对,后放甲基,共10种,第二种情况是苯环上放两种基团,-OH和-CH2CHO,邻间对,共3种,所以W 的可能结构有13种;符合①遇FeCl3 溶液显紫色、②属于芳香族化合物、③能发生银镜反应其中核磁共振氢谱显示有5 种不同化学环境的氢、峰面积比为2:2:2:1:1要求的W 的结构简式:
,化合物W 的相对分子质量比化合物C 大14,W比C多一个CH2,遇FeCl3 溶液显紫色含有酚羟基,属于芳香族化合物含有苯环,能发生银镜反应含有醛基,第一种情况是苯环上放三种基团,醛基、羟基和甲基,先固定醛基和羟基的位置,邻间对,后放甲基,共10种,第二种情况是苯环上放两种基团,-OH和-CH2CHO,邻间对,共3种,所以W 的可能结构有13种;符合①遇FeCl3 溶液显紫色、②属于芳香族化合物、③能发生银镜反应其中核磁共振氢谱显示有5 种不同化学环境的氢、峰面积比为2:2:2:1:1要求的W 的结构简式:![]() ,故答案为:13;
,故答案为:13;![]() 。
。
(5)根据题目已知信息和有关有机物的性质,用甲苯和乙醛为原料制备 的合成路线:
的合成路线:
 ,故答案为:
,故答案为: 。
。

【题目】能源、环境与生产生活和社会发展密切相关。
(1)工业上利用CO和H2在催化剂作用下合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) ,已知反应中有关物质的化学键键能数据如下表所示:
CH3OH(g) ,已知反应中有关物质的化学键键能数据如下表所示:
化学键 | H—H | C—O | C≡O | H—O | C—H |
E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
则 CO(g)+2H2(g) ![]() CH3OH(g) △H=__________kJmol-1
CH3OH(g) △H=__________kJmol-1
(2)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池。如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。

B极为电池______极,B极的电极反应式为_________________________________。
(3)参考合成反应CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数,回答下列问题:
CH3OH(g)的平衡常数,回答下列问题:
温度/℃ | 0 | 50 | 100 | 200 | 300 | 400 |
平衡常数 | 667 | 100 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
①该反应正反应是 ___________(填“放热”或“吸热”)反应;
②在T℃时,1L密闭容器中,投入0.1molCO和0.2molH2,达到平衡时,CO转化率为50%,则T=__________℃。
(4)CH3OH也可由CO2和H2合成。在体积为1L的密闭容器中,充入lmolCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH= — 49.0kJ/mol,测得CO2和CH3OH(g)浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH= — 49.0kJ/mol,测得CO2和CH3OH(g)浓度随时间变化如图所示。
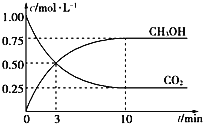
①该反应的平衡常数表达式为K=_______;从反应开始到10min,v(H2)=_____mol/(L·min);
②下列情况能说明该反应一定达到平衡状态的是___________(填字母)
A.v(CO2)消耗 = v(CH3OH)生成
B.气体的密度不再随时间改变
C.CO2和CH3OH的浓度之比不再随时间改变
D.气体的平均相对分子质量不再随时间改变
③为了加快化学反应速率且使体系中气体的物质的量增大,只改变下列某一条件,可采取的措施有__ (填字母)
A.升高温度 B.缩小容器体积
C.再充入CO2气体 D.使用合适的催化剂
④相同温度下,在另一个容积为1 L的密闭容器中充入2mol CH3OH(g)和2molH2O(g),达到平衡时CO2的浓度_______(填“>”、“ <”或“=”)0.25mol/L。



