题目内容
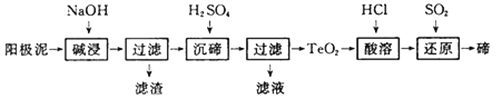
【题目】碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(含有质量分数为8%的TeO2、少量Ag、Au)为原料制备单质碲的一种工艺流程如下,(已知TeO2微溶于水,易溶于强酸和强碱),下列有关说法不正确的是
A. 将阳极泥研磨、反应适当加热都有利于提高“碱浸”的速率和效率
B. “碱浸”时发生主要反应的离子方程式为TeO2+2OH-=TeO32-+H2O
C. “沉碲”时为使碲元素沉淀充分,应加入过量的硫酸
D. 若提取过程碲元素的回收率为90%,则处理1kg这种阳极泥最少需通入标准状况下SO2 20.16L
【答案】C
【解析】
本流程目的为利用阳极泥(含有质量分数为8%的TeO2、少量Ag、Au)为原料制备单质碲,所以先要进行除杂,最后提取Te。根据TeO2微溶于水,易溶于较浓的强酸和强碱,流程中先加碱溶,过滤除去杂质,得到溶液,再加硫酸沉降经过滤得到TeO2沉淀,再用盐酸溶解生成四氯化碲,再用二氧化硫还原制成碲单质,以此解答。
A、研磨增大接触面积,加热均能提高“碱浸”的速率和效率,故A正确;
B、由已知信息可知,TeO2微溶于水,易溶于强酸和强碱,是两性氧化物,与氢氧化钠发生类似氧化铝与氢氧化钠的反应,生成TeO32-,离子方程式为TeO2+2OH-=TeO32-+H2O,故B正确;
C、由已知信息可知,TeO2易溶于强酸和强碱,在沉降的过程中,硫酸若过量,可能导致TeO2的溶解,造成产品的损失,故C错误;
D、1kg阳极泥中含TeO2的质量为1000g×8%=80g,碲元素的回收率为90%,则有80g×90%=72g的TeO2被还原。每摩尔TeO2得4mol电子,每摩尔SO2失去2mol电子,则有关系式:1TeO2~2SO2,V(SO2)=![]() ×2×22.4L/mol=20.16L,故D正确。
×2×22.4L/mol=20.16L,故D正确。
答案选C。

 名师点拨卷系列答案
名师点拨卷系列答案【题目】为了防止氮氧化物对空气的污染,人们采取了很多措施。
(1)如用CH4催化还原NO2可以消除氮氧化物的污染,发生的反应如下: CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1。
N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1。
①下列有关说法正确的是_________。
A.在容器中充入1mol CH4和2 mol NO2,当体系中n(CH4)/n(NO2)比值不随时间变化时,反应达到平衡状态
B.恒温恒容时,当混合气体的密度不随时间变化时,该反应达到平衡状态
C.体系达到平衡后,升高温度,体系中的混合气体的平均相对分子质量增大
D.恒温恒压时,充入CH4有利于提高氮氧化物的转化率
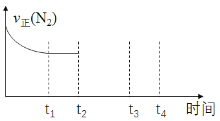
②在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态。请在右图中补充画出从t2到t4时刻v正(N2) 随时间的变化曲线:____________
(2)现有的汽车尾气处理的原理是:NO(g)+2CO(g)![]() N2(g) +2CO2(g),通常使含适当比例的NO、CO尾气通过装有高效催化剂的处理装置。请根据以下相关数据,分析仅使用催化剂能否有效消除NO、CO尾气污染___________。
N2(g) +2CO2(g),通常使含适当比例的NO、CO尾气通过装有高效催化剂的处理装置。请根据以下相关数据,分析仅使用催化剂能否有效消除NO、CO尾气污染___________。
反应 | 25℃时的平衡常数 | 焓变 |
反应I:2NO(g) | K1=1×1030 | △H=-180.5kJ/mol |
反应II:2CO2 (g) | K2=4×10-92 | △H= +566.0kJ/mol |
(3)用NH3催化还原NOx也可以消除氮氧化物的污染,其反应原理为:NO(g) +NO2(g)+2NH3(g)![]() 2N2(g) + 3H2O(g)。一定温度下,在某恒定压强为P的密闭容器中充入一定量的NO、NO2和NH3,达到平衡状态后,容器中含n(NO)=a mol,n(NO2)=2a mol,n(NH3)=2a mol,n(N2)=2b mol,且N2(g)的体积分数为1/3,请计算此时的平衡常数Kp=________________。(用只含P的式子表示,且化至最简式)。(备注:对于有气体参加的反应,可用某组分的平衡分压代替物质的量浓度计算平衡常数,记作KP。如p(NO2)为NO2的平衡分压,p(NO2)=x(NO2)p,p为平衡总压,x(NO2)为平衡体系中NO2的物质的量分数。)
2N2(g) + 3H2O(g)。一定温度下,在某恒定压强为P的密闭容器中充入一定量的NO、NO2和NH3,达到平衡状态后,容器中含n(NO)=a mol,n(NO2)=2a mol,n(NH3)=2a mol,n(N2)=2b mol,且N2(g)的体积分数为1/3,请计算此时的平衡常数Kp=________________。(用只含P的式子表示,且化至最简式)。(备注:对于有气体参加的反应,可用某组分的平衡分压代替物质的量浓度计算平衡常数,记作KP。如p(NO2)为NO2的平衡分压,p(NO2)=x(NO2)p,p为平衡总压,x(NO2)为平衡体系中NO2的物质的量分数。)
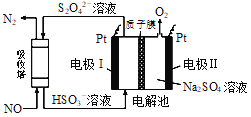
(4)用间接电化学法对大气污染物NO进行无害化处理,其原理示意如图(质子膜允许H+和H2O通过),电极I发生的电极反应为_________________________。