题目内容
已知A、B、C、D、E、F是含有同一种元素的化合物,其中F能使红色湿润石蕊试纸变蓝色,它们之间能发生如下反应:
①A+H2O→B+C ②C+F→D ③D+NaOH→F+E+H2O
(1)写出它们的化学式:D
(2)写出①反应的化学方程式:
(3)写出反应③的离子方程式:
(4)工业生产C的过程中有如下一步反应:即F经催化氧化生成B和H2O,写出该步反应的化学方程式:
①A+H2O→B+C ②C+F→D ③D+NaOH→F+E+H2O
(1)写出它们的化学式:D
NH4NO3
NH4NO3
,FNH3
NH3
.(2)写出①反应的化学方程式:
3NO2+H2O═NO+2HNO3
3NO2+H2O═NO+2HNO3
,此反应中氧化剂是NO2
NO2
,还原剂是NO2
NO2
.(3)写出反应③的离子方程式:
NH4++OH-
NH3↑+H2O
| ||
NH4++OH-
NH3↑+H2O
.
| ||
(4)工业生产C的过程中有如下一步反应:即F经催化氧化生成B和H2O,写出该步反应的化学方程式:
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
分析:A、B、C、D、E、F是含有同一种元素的化合物,其中F能使红色湿润石蕊试纸变蓝色,则F是NH3,它们之间能发生如下反应:③D+NaOH→F+E+H2O,说明D是铵盐,E为钠盐,且A、B、C、D、E、F是含有同一种元素的化合物,则E是NaNO3,D是NH4NO3,根据②C+F→D知,C是HNO3,根据①A+H2O→B+C知,且A和B、C都含有同一种元素,则A是NO2,B是NO,根据物质的性质分析解答.
解答:解:A、B、C、D、E、F是含有同一种元素的化合物,其中F能使红色湿润石蕊试纸变蓝色,则F是NH3,它们之间能发生如下反应:③D+NaOH→F+E+H2O,说明D是铵盐,E为钠盐,且A、B、C、D、E、F是含有同一种元素的化合物,则E是NaNO3,D是NH4NO3,根据②C+F→D知,C是HNO3,根据①A+H2O→B+C知,且A和B、C都含有同一种元素,则A是NO2,B是NO,
(1)通过以上分析知,D和F分别是NH4NO3、NH3,
故答案为:NH4NO3;NH3;
(2)二氧化氮和水反应生成一氧化氮和硝酸,反应方程式为:3NO2+H2O═NO+2HNO3,该反应中N元素化合价由+4价变为+2价和+5价,所以此反应中氧化剂NO2,还原剂是NO2,
故答案为:3NO2+H2O═NO+2HNO3;NO2;NO2;
(3)硝酸铵和氢氧化钠反应生成氨气、硝酸钠和水,离子反应方程式为NH4++OH-
NH3↑+H2O,
故答案为:NH4++OH-
NH3↑+H2O;
(4)工业生产HNO3的过程中有如下一步反应:即NH3经催化氧化生成NO和H2O,反应方程式为:
4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O.
(1)通过以上分析知,D和F分别是NH4NO3、NH3,
故答案为:NH4NO3;NH3;
(2)二氧化氮和水反应生成一氧化氮和硝酸,反应方程式为:3NO2+H2O═NO+2HNO3,该反应中N元素化合价由+4价变为+2价和+5价,所以此反应中氧化剂NO2,还原剂是NO2,
故答案为:3NO2+H2O═NO+2HNO3;NO2;NO2;
(3)硝酸铵和氢氧化钠反应生成氨气、硝酸钠和水,离子反应方程式为NH4++OH-
| ||
故答案为:NH4++OH-
| ||
(4)工业生产HNO3的过程中有如下一步反应:即NH3经催化氧化生成NO和H2O,反应方程式为:
4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
点评:本题以N元素为载体考查了含氮化合物的推断,以F为突破口结合物质间的转化分析推断,难度不大,注意多总结归纳基础知识,知道常见物质的性质.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
已知A、B、C、D分别是Cu、Ag、Fe、Al四种金属中的一种.已知①A、C均能与稀硫酸反应放出气体;②B与D的硝酸盐反应,置换出单质D;③C与强碱反应放出气体,由此可以推断A、B、C、D依次是( )
| A、Fe、Cu、Al、Ag | B、Al、Cu、Fe、Ag | C、Cu、Ag、Al、Fe | D、Ag、Al、Cu、Fe |

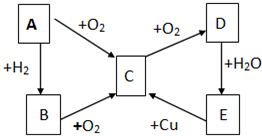 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素. (Ⅰ)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答:
(Ⅰ)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答: